 |
 |
 |
 |
1 ... 18 19 20 21 22 23 24 ... 48 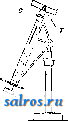 А Фиг. 1. растворяясь затем при выделении серы и окиси сурьмы. КОН извлекает из П. сернистую сурьму, осаждаемую к-тами в виде по-меранцево-жеЛтого осадка. П. встречается во. всех серебряных месторождениях, иногда в весьма больших количествах. Сюда относятся: 1) Гарц, Вестфалия, Рудный кряж в Германии, 2) Богемия, 3) С. и Ю. Америка, 4) Алтай в СССР. Одинаковый состав СП. имеет пиростильпнит (огненная обман к а) моноклинной системы; кри-сталлйзуетсй в виде мелких и тонких табличек померайцево-желтого или красно-бурого цвета; тв. 2; уд. в. 4,3. Лит.: Б о .71 д ы р е в А. К., КурсОписатель-UOU йпшерклогии, кыя. 1, Д., 1926. И. Мельников. ПИРГЕЛИОМЕТР, прибор для измерения тепловой энергии солнечного излучения (см. -Дктмнолгетрмя); предложен в 1837 г. Пулье (Pouillet), который произвел с ним ряд актинометрич. исследований. Прибор состоит (фиг. 1) из тонкостенного цилиндрич. сосуда А, верхняя поверхность к-рого закопчена. В сосуд налита вода, и он представляет собою не что иное, как калориметр. Внутри труб-1си D находится термометр Т для определения i° воды. Сначала прибор направляют в противоположную сторону ОТ солнца и измеряют паденир Г в течение 5 мин. Затем вос-принимаюп];ую часть 4 направляют пртю па солнце й отмечают повышение температуры также в те-чеш1е 5 мин. После этого повторяют опять первую операцию. Зная теплоемкость калориметра, можно определить обш;ее количество тепла, получаемого единицей поверхности в единицу времени. Результаты, полученные Пулье, очень хорошо согласуются с современными. Видоизменением описанного прибора является так называемый серебряный П., предложенный Смит-сонианской обсерваторией. Прцбор! этот (фйг. 2); имеет Ши-рокЬе распространение, особенно в Америке и отчасти в Европе. В серебряном диске А сделано отверстие, через к-рое входит шарик термометра, трубка которого В согн;5 га под прямым углом. Отверстие выложено тонкой стальной пластинкой и в него налита ртуть для лучшей передачи тепла. Серебряный диск заключен в латунную цилиндрич. коробку С, к-рая в свою очередь вделана в деревянную оправу D для предохранения инстру-меета от внешних t°-Hbix изменений. Пучок солнечных лучей входят через коробку Е с рядом диафрагм F, так что лучи падают только на диск. При помойи диафрагмы If можно по желанию или открыть или за- 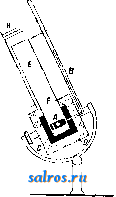 Фиг. %. крыть отверстие трубкиЕ. После установки прибора на солнце открывают диафрагму так, что лучи падают на А. Достаточно 100 ск. времени, чтобы установилось определенное тепловое равновесие. Из наблюдаемого при этом повышения f° можно вьгее-сти значение интенсивности со.тнечного излучения. Несмотря на сравнительную простоту конструкции, результаты наблюдения получаются с большой степенью точности. П. системы проф. В. А. Mиxeль-c о н а имеет широкое применение в Запад-  Фиг. 3. ной Европе и в СССР. Он состоит (фиг. 3) из биметаллич. пластинки А, закрепленной с одного конца и подвергающейся радиации солнца через отверстие D. Перемещение свободного конца Р наблюдается с помопцю микроскопа М. Прибор предварительно калибрируют, производя одновременные наблюдения с абсолютным инструментом. Самые наблюдения производят, отмечая степень отклонения Р при открытом и закрытом отверстии jD. Вс.тедствие малой теплоемкости пластхшки J. инструмент отличается большой чувствительностью, и с помощью его можно очень быстро определить солнечную радиацию. Абсолютный водоструйный П. Abbota и FowleH (фиг. 4) представляет со-бо10 комбинацию черного тела и калориметра особой системы. Главным нововведением, примененным в этом приборе; является камера, в которой полностью абсорбируется энергия солнечных лучей, т. ч. нет необходимости вводить особые поправки на отражение лучей. Солнечные лучи, пройдя через трубку В и отверстие С, входят в воспринимающую камеру At конич. основанием Л, к-рая служит черньш телом. В то же время через трубку Е идет ток воды, омьшаюпщй прибор; перед воспринимающей камерой 1°  Фilг. 4. воды тщательно измеряется с помощью термоэлемента Dj, после чего вода циркулирует вокруг камеры; здесь она нагревается под влиянием тепловой энергии, встащившей в камеру, а затем вода выводится наружу через отверстие F. Перед выходом Г воды вновь измеряется с помощью второго термоэлемента £).. Вода циркулирует по особым спиральным каналам. Для предохранения от изменения внешней 1° весь прибор заключен в дьюаровский сосуд К. Таким образом изменешге V в водяной струе, псир-  Фиг. 5. кулирующей около прибора, служит мерой солнечной инсоляции, определяемой с помощью измерения количества электрической энергии, пропускаемой через манганиновую обмотку вокруг конуса Н и нагревающей как воспринимающий сосуд, так и циркулирующую воду. Компенсационный П. сист. Онг-стрема (фиг. 5) представляет прибор для абсолютного определения интенсивности сол-печного излучения. Он состоит из двух зачерненных пластинок S я Т одинакового размера, к которым прикреплены снаи двух термоэлементов а vl Ь. Когда пластинка S подвергается действию солнечного нагр е-вания, а пластинка Г, защищенная ширмочкой от солнца, остается при постоянной t°, в цепи возникает термоток, и стрелка гальванометра Gx отклонится. Если пластинку Т нагреть до одинаковой 1° с пластинкой S, термоток в цепи прекратится и стрелка гальванометра Gi возвратится в нулевое положение. Нагревание осуществляют с помощью электрич. тока от батареи Е, быстро подбирая надлежащее сопротивление R и определяя силу тока гальванометром Ga- Эти измерения дают все необходимые данные для определения солнечной радиации. Некоторые виды пиргелиометров сконструированы для непрерьтной регистрации солнечной инсоляции. Лит.: КлоссовскийА., Метеорология, Общий курс, ч. 1, Метеорология статическая, Одесса, 1908; МихельсонВ. А., 35 лет актинометрич. исследований, Записки Моск. метеорол. общества , М., 1928, вып. 3; Инструкция для производства наблюдений пластинчатым актинометром Михельсопа, Л., 1929; ВейнбергБ.П., Желтый уголь. Мощность лучистой энергии солнца, Л., 1929; oAstrophyslcal Journal*, Chicago, 1911. В. Пришлецов. ПИРИДИН, CgHgN, бесцветная прозрачная, обладающая резким специфическим запахом, жидкость. = 0,978; 115,1°, 38,2°, скрытая теплота испарения (при 115,5°) 101,4 са1/г, удельная теплоемкость (в пределах 21108°) 0,431; вязкость при 25° 0,0088. В воде, спир-сн те и эфире пиридин растворим во всех отношениях; с водою он дает гидрат CsHgN-SHaO, кипя-пщй при 92-93°. П. сильно гигроскопичен. Он является хорошим растворителем для многих органических веществ; хлористая и хлорная медь, хлористый цинк, хлорная ртуть, хлористое серебро, азотнокисл. свинец легко растворяются в П. Хлористая ртуть при прибавлении П. мгновенно разлагается на ртуть и хлорную ртуть, переходящую в раствор. В химическом отношении П. представляет слабое основание, не меняющее цвета лакмуса, но образующее с сильными минеральными кислотами соли, легко растворимые в воде. Подобно аммиаку П. образует ряд двойных и комплексных со-.яей, например (C5H6N-HCl)2PtCl4. Пиридин очень стоек по отношению к окисляющим у по/i4cH НСпб 21 реагентам и к действию высоких t°; при кипячении с азотной или хромовой кислотами он не разлагается. При действии водорода в присутствии никеля при t° 180-250° П. в большей части остается неизмененным; при восстановлении натрием в горячем растворе в абсолютном этиловом спирте - дает полностью гидрированное соединение п и-перидии CbHiiN. При нагревании выше 300° с конц. подистоводсродной кислотой п. расщепляется, давая нормальный пентан и аммиак; при нагревании до 330° с нитрующей смесью (HNO3 -f H2SO4) дает нитро-пиридин (игольчатые кристаллы 41°, t°Kurn 216°); при кипячении с конц. серной к-той дает сульфосоединение. Находится П. гл. обр. в продуктах пиролиза каменного угля, бурого угля, торфа, лигнита и древесины; пиридиновое гетероциклическое ядро входит в состав многих алкалоидов. В иромьниленном масштабе П. добывается в смеси с его гомологами из легких и средних фракций каменноугольной смолы (см. Пиридиновые основания). Многочисленные синтезы П. освещены в специальной литературе. Пиридин применяется в качестве растворителя многих органич. веществ как в технике (напр. для растворения каучука), так и для целей анализа, например для определения свободных углеводородов в каменноугольной смоле; при органич. синтезах П. служит катализатором (например при окислении ацетальдегида в перекись ацетила), также в качестве среды для сохранения активного никелевого катализатора: Ni под слоем П. долго сохраняет активность. П. пользуются как средством, связывающим соляную кислоту (напр. при ацетилировании целлюлозы помощью хлористого ацетила); П. применяется также для очищения индиго, для денатурации винного спирта и в качестве инсектисида, защищающего виноград от виноградной тли. Лит.: Чичибабин А. Е., Основные начала органической химии, 3 изд., М.-Л., 1931; Н о 11 i п s С, The Synthesis of Nitrogen Ring Compounds Containing a Single Hetero-Atom (Nitrogen), L., 1924; Meyer V. u. Jacob son P., Lehrb. d. organ. Chemie, B. 2, ТеП 3, 2 Aufl., В., 1923. Ф. Рыбкин. ПИРИДИНОВЫЕ ОСНОВАНИЯ, производные пиридина (см.), получаемые из продук-. тов перегонки каменноугольной смолы (см. Коксобензольпое производство, переработка каменноугольной смолы), в к-рой находится смесь пиридина с его гомо.чогами. П. о. обнаружены также в буроугольном и древесном дегте и в торфе. Кроме самого пиридина, составляющего не менее 50% всей смеси, там находятся 2-, 3-, 4-монометилпиридины (а-, Д-,у-пи-колины) CHa-CsHiN уд. в. 0,961-0,976 при 0°, t\un. от 133,5°; 2,4-, 2.5-, 2,6-, 3,4-, 3,5-диметилпиридины (а, /5-, а, а, а'-, /5, у-, j8, /З'-лутидины) (CHagCgHaN удельн. в. ~0,95 и 142-164°; 2,4,5- и 2, 4, 6-триметил- пиридины [коллидины (CH3)3C5H2N уд. вес ~0,92 и 165-172°]. По свойствам гомо- логи пиррщина подобны самому пиридину. Среднее содержание П. о. в каменноугольной смоле по данньш Lunge - КбЫег [] 0,05 - 0,1%; Warnes дает следующие средние данные для содержания П. о.: в однократно перегнанном бензоле - легких оснований (90° до 140°) 0,75%, тяжелых 0,057%, в один раз перегнанной сольвентнафте: легких 4,01 %,тяжелых 1,19%; всего в среднем*0,12%. Смолы, получаемые при низкотемпературной карбонизации торфа и лигнита, более богаты П. о., чем каменноугольная смола, получаемая при высоких t°. Главная масса П. о. находится в т. н. ф е-нольном масле, фракции каменноугольной смолы, перегоняющейся в пределах 180-220°; разница в Г„ .П. о. и t° . этой фракции объясняется тем, что П. о. дают с фенолами соединения типа CeHsOH-CsHgN и (CgHgOa-CsHsN, столь прочные, что при прибавлении к маслам, содержащим их, серной кислоты, они не вполне разлагаются; этим обусловливается необходимость предварительного удаления из масла фенолов промывкой щелочью. После выделения фенолов П. о. связьшаются серной к-той крепостью 30-35%. Полученный раствор сульфатов П. о. для удаления увлеченных масел продувается острым паром или разбавляется равным по объему количеством воды. Для вьщеления П. о. из сульфатов применяются несколько способов, из к-рых главнейшими являются следующие. 1) Осветленные сульфаты П. о. смешиваются с гашеной известью, загруженной предварительно в аппарат, в который подведен острый пар; после перемешивания содержимого в аппарат пускают острый пар, с к-рым и отгоняются вьщелившиеся П. о. Отгон в начале гонки д. б, совершенно прозрачен и лишь во второй половине гонки появляется муть, вызванная наличием в погоне тяжелых П. о., трудно растворимых в воде. Отгон ведут обычно до тех пор, пока взятая проба не будет содержать около 1 % П. о.,что грубо определяется след. обр.: пробу отгона смешивают в дел^ельной воронке 2 раза с равным объемом раствора едкого натра NaOH уд. веса 1,45, сливают нижний тяжелый слой щелочи и переливают выделргеши-еся П. о. в измерительный цилиндр. В среднем полученный водный раствор И.о. содержит их в количестве 35-40%. Для вьщеления их прибавляют раствор NaOH уд. веса 1,30-1,45 с таким расчетом, чтобы получаемый разбавленный раствор щелочи имел уд. вес не менее 1,15, т. к. в растворах большего уд. веса П. о. не растворяются, а в более слабых растворяются. Для окончательной сушки прибавляют к выделенным П. о. твердый NaOH или его раствор уд. в. 1,45. Если на смолоперегонном з-де разложение фенолята производится углекислотой, в результате чего пол^гаастсяуглекислый натрий, последний также м. б. применен для вьщеления П. о. из воды (но не для сушки). Высушенные П. о., содержащие до 4% влаги, подвергаются ректификации (сравнительно грубой), причем собирается фракция, 90% к-рой перегоняется до 140 или до 160°. Во избежание плотного оседания на дне куба известкового шлама необходимо выгружать последний сразу после прекращения отгонки. 2) К раствору сернокислых П. о. прибавляют аммиачную воду (около 16% NH3) до начала вьщеления свободных П. о.; примешанные масла при этом отделяются. Осветленный раствор загружается в освинцован- ный сатуратор и через него пропускается аммиачный газ из аммиачной колонны, который образует с серной к-той сульфат аммония. Операция ведется при охлаждении, для чего сатуратор снабжен свинцовьпл змеевиком. После окончания операции жидкости в сатураторе разделяются и верхний слой, заключающий П. о., осушается щелочью, как указано для первого способа. 3) Третий способ основан на способности П. о, давать гидраты типа CgHgN 3 HgO, перегоняющиеся в пределах от 93 до 96°. Осветленный раствор сернокислых П, о. обрабатьшается раствором NaOH до полной нейтрализации всей серной к-ты. Полученную смесь П. о. и сульфата натрия загружают в куб, снабженный ректификационной колонной, и нагревают сперва глухим паром, а затем острым и собирают фракцию 93-96°. Прп превышении последней погон начинает мутнеть вследствие примеси тяжелых П. о. Отгон конденсируется и первая фракция гидратов отводится в мешалку, а вторая, содержащая тяжелые П. о проводится через флорентийскую склянку для отделения П. о. от воды. Гидраты П. о. в мешалке осушаются добавкой крепкого раствора NaOH, Суще-ственньш недостатком этого метода является значительный расход NaOH, к-рый выходит из производства в виде отброса-сульфата натрия. Растворы щелочи, полученные при осушке П. о используются как во всех способах, напр. для выделения фенолов из масел. Преимущество этого способа-получе-mie очень чистых П. о тяжелых 99-99,5%, легких 98-99%.4) Сернокислые П, о, разлагаются крепкой аммиачной водой в присутствии бензола, к-рый является для них хорошим растворрггелем. Бензольный раствор подвергается ректификации, при к-рой помимо бензольного и пиридинового погонов получаются промежуточные, нуждающиеся во вторичной перегонке, (При всех работах с П,о. необходимо обращать серьезное вш-мание на герметичность всей аппаратуры во избежат^е проникновения в рабочее помещение ядовитых пиридиновых паров.) Испытания готового продукта. Согласно герм, нормам П. о. не должны содержать более 10% (иногда 7%) воды. Содержание воды определяется в специальной бюретке на 50 см, в к-рую наливают 23 см раствора NaOH уд, веса 1,40 и затем 25 см испытуемой пробы; прирост в объеме щелочи после энергичного встряхивания и отстаивания показьшает содержание влаги. Продукт может иметь окраску не сильнее чем 2 см N раствора иода в 1 л дистиллированной воды; 20 сми. о. должны давать прозрачный раствор в 40 см воды. Аммиак должен отсутствовать. 10 см 1 %-ного (по объему) раствора П. о. должны давать белый осадок с реактивом Несслера. 10 см 1 %-ного раствора П. о., смешанные с 5 см 5%-ного водного раствора хлористого кадмия, после энергичного встряхивания должны давать почти немедленно отчетливо кристаллический осадок. До 140° (или до 160°) должно перегоняться 90%. Для обнаружения П. о. служат обычно следуюпще реакции. К 1 см П. о., растворенных в 10 см дистиллированной воды, добавляется Vj N HgSO до появле- 4:11 ПИРИТ ния синего окрашивания на конго. Минимум к-ты 10 см. Очень чувствительной пробой на П. о. яв.тяется следующая. К воде, содержащей П. о., добавляют несколько капель анилина и ничтолшое количество свежеприготовленного бромистого циана: сразу появляется красное окрашивание и выделяются кристаллы а-анилидофенилдигидро-пиридинбромида. Эта проба обнаруживает П. о. Б разбавлении 1 : 350 ООО. -Ямт.: 1) Lunge О. и. КбЫег Н., Die Industrie des Steinkoblenteers u. Ammonlaks, 5 Auflage, B. 1, Brschw., 1912; Warnes A., Coal Tar Distillation a. Working-up Tar Products, 3 ed., L., 1923.- В u n b u r у H. a. D a v i d s о n A., The Industrial Applications of Coal Tar Products, L., 1925. Ф. Рыбкин. ПрименениеП о. обусловлено главн. образом их способностью растворять многие органич. и неорганич. вещества и тем, что П. о. являются слабыми основаниями, вследствие чего применяются для нейтрализации кислых веществ. Главное применение находит важнейшая составная часть П. о .-пиридин (см.) чистый и технический. В ани л окрасочной промышленности П.. о. применяют для очистки антрацена от фен-антрена и карбазола, для разделения 1,5-и 1,8-динитронафталина, для переведения интроантрахинона в оксиантрахинон, для очистки синтетического индиго и кубовых красителей и приготовления основных и три-фенилметановых красителей. П. о. применяются для облагораживания хл.-бум. волокна и в качестве добавки в целлюлозные .таки. Одно время П. о. применялись как средство, связывающее соляную кислоту при ацетилировании целлюлозы хлористым ацетилом по способу Воля. В крашении П. о. применяются вместе с ароматич. сульфоки-слотами в качестве эмульгирующего и смачивающего средства и как добавка, облегчающая крашение ацетата целлюлозы основными красителями. В кожевенном производстве П. о. совместно с другими аминами и сульфидами натрия и аммония применяются для сгонки волоса и как нейтрализующее средство при дублении кожи и мехов. П. о. рекомендованы для разделения ми-неральЯьгх масел и их дистиллатов на легкие и тяжелые части. П. о., в особенности их высшие фракции, в силу их токсичности применяются в чистом виде или в комбинации с другими веществами в качестве ин-сектисидов: вместе с калийным мылом или в форме нафтеновокислых, смоляно- и ду-бильнокислых солей или в комбинации с динитрохлорбензол ом и хлорпикрином, в ica-честве сильно действующего инсектисид-ного средства предложен к употреблению а-аминопиридин. П. о. обладают консервирующим действием и применяются для консервирования дерева, в частности пропитки шпал, в фотографии пиколиновая фракция П. о. применяется как компонент в сенси-билизаторных смесях (пинацианоль, пина-флаволь). Концентрированный раствор двойных соединений дипиридинбетаина с хлористым натрием и кальцием имел применение одно время в качестве суррогата глицерина. П. о. предложены для извлечения литиевых солей, а также получения лития. Главна.я масса П. о. однако применяется для денатурации спирта. о. Зейда. ПИРИТ, серный колчедан, железный колчедан, минерал группы серного колчедана, относится к двусернистым соединениям ковких металлов общей ф-лы RSg. Принадлежит к дидодекаэдрич. виду симметрии кубич. системы; отличается богатством форм (до 87) и разнообразием комбинаций. Грани куба и октаэдра в кристаллах весьма часто покрыты штрихами. Часто наблюдаются двойники. Спайность по кубу весьма несовершенная. Излом раковистый, неровный. Хрупок. Цвет бледный латунно-желтый, иногда почти золотожелтый, редко с побежалостями (иногда приобретает бурую побежалость вследствие образования на поверхности водной окиси железа). Черта (на фарфоровой пластинке) от зеленовато-черной до буровато-черной. Блеск металлический. Плохой проводник электричества. Не действует на обыкновенную магнитную стрелку, весьма слабо на астатическую. Химич. состав FeSa (46,67% Fe; 53,33% S), иногда содержит Au, Ag, Си, Mn, а также As, Со, Ni, Zn, Tl, Se; Au и Ag из некоторых П. с выгодой извлекаются. В недрах земли, как и на поверхности, легко переходит в бурый железняк (см.). При нагревании в колбе возгоняется S и остается FeS; этим способом извлекают иногда из П. серу в больших количествах. При нагревании в открытой стеклянной трубке выделяется SO а (характерный запах). Перед паяльной трубкой (см.) П. горит голубым пламенем при вьщелении SOa, причем остается красная FegOa. Выделяющийся сернистый ангидрид (SOa) при обжиге П. используют для приготовления HaSOi, а остающуюся FcaOg для приготовления красок. В восстановительном пламени паяльной трубки П. сплавляется в черный магнитный королек. В HNO3 растворяется при выделении S. К-ты НС1 и HF на П. действуют чрезвычайно слабо. Тв. 6-6,5; уд. в. 4,95-5,10. П. наиболее распространенный из сернистых металлич. минералов. Встречается в кристаллах, вросших в породу поодиночке или соединенных в правильные, округленные группы, или в виде друзов, дендритов, конкреций, или еще чаще в виде сплошных масс различной структуры (шаровидной, почковидной, гроздевидной). Эти образования имеют внутри лучистое, тонкозернистое или плотное сложение. В пластовых и жильных месторождениях П. встречается в сопровождении медного колчедана, цинковой обманки, свинцового блеска, мышьякового колчедана, серебряной руды, магнитного железняка, железного блеска, оловянного камня, шпатового железняка, а также особенно часто с кварцем в различных месторождениях. Кроме того П. встречается в древнейших изверженных горных породах (гранит, сиенит, диорит), в новейших (трахит, андезит), в кристаллич. сланцах, известняках, глинистых сланцах, в каменных и бурых углях, а также в других продуктах органич. происг-хождения (янтарь) В палеозойских формациях и кристаллич. сланцах П. образует значительные массы в сопровождении медного колчедана (хорошая медная руда), свинцового блеска и цинковой обманки, а также и. золота (в кварцевых золотоносных рудах). П. редко встречается в виде псевдоморфоз по форме других минералов (магнитный колчедан, плавиковый шпат и др.), но весьма часто является оруденяюш;им веществом ископаемых остатков, удерживая форму способных к сохранению твердых частей животных (раковины) и растительных организмов. В сплошных и плотных мДссах П. часто бывает трудно отличить от реже встречаемого марказита, который тождествен по составу с П., но быстрее подвергается выветриванию, превращаясь в железный купорос с образованием H2SO4. Д. легко выветривается, давая различные продукты преобразования: лимоиит (см.), безводную окись железа, железный купорос. Если П. вкраплен в глины, то выделяющаяся при выветривании его SO3 образует А13(804)з.переходяпщй по прибавлении солей в квасцовые глины, служащие для извлечения квасцов. П. применяется для получения железного купороса, квасцов, серы, серной к-ты. В последнем случае он является главньш материалом, т. к. из него получается ок. 0,9 всего количества применяемой в технике HaS04 (только 0,1 добывается из серы). Остатки от упомянутых процессов используют для приготовления дешевых желтой и красной красок, а также для извлечения меди и железа (см. Пиритовые огарки). Кроме того пирит находит применение как флюс при некоторых заводских процессах. Золото-и серебросодержащие руды пирита служат для извлечения золота и серебра. В качестве железной руды цирит не применяется, так как дает содержащее серу красноломкое железо. и. Мельников. П. играет настолько серьезную роль в мировой промышленности, что на 14-м Международном конгрессе был произведен подсчет мировых ресурсов его, давший данные, приведенные ниже в таблице (ст. 414). Первое место по запасам серньгх колчеданов занимает Испания (знаменитое месторождение Рио Тинто), обладающая почти половиной мировых запасов; Япония обладает 1/в частью мировых запасов. И по добыче серного колчедана Испания стоит также на первом месте; затем идут в убывающем порядке Норвегия, Италия, Япония, Германия, Португалия, Франция, США, Кццр и СССР. Из многочисленных месторождений П. в СССР наибольшее значение имеет Урал (комбинаты Богомольский, Калатин-ский и Карабашский); затем закавказские месторождения в Армянской (Аллавердский, Шамблугский, Ахтальский, Сисимаданский, Танзутский и др.) и Азербайджанской ССР (рудники Чирагидзорский,-Кёдабекский и др.); в Ленинградской области-Борович-ский комбинат. В Московсйой области производится добыча П. попутно'с добычей угля (Тульский, Рязанский, Калужский, Бобр иковский и другие районы). Кроме того необходимо отметить месторождения П. на Алтае и в Казакстаие близ Байконура (на р. Терс-Бутак). Несмотря на многочисленность месторождений П. в Союзе эксплоата-ция их далеко не всегда возможна и выгодна вследствие их географического положения (дальность перевозок)!. Так, большинство месторождений (Урал, Кавказ) находится Мировые запасы серного колчедана по подсчету 14 Геологического конгресса (в тыс. та). Запас м Я i ? 3 m и S О со о л и Всего Евро па Испания . . . Норвегия . . . Италия .... СССР (Урал) . Португалия . Германия. . . Швеция .... Румыния . . . Франция . . . Греция .... Кипр..... Австрия . . . Финляндия. . Польша .... 272 731 40 473 904 338 09 L ]92 581 253 519 500 i 147 562 15 7i5 10 204 25 077 14 870 6 464 3 750 2,297 5 000 2 200 2 ООО 65 ООО Очень больш. 820 1 550 15 000 14 000 700 1 - Незяа-1 485 293 I 56 188 j 19 928 35 965 , 22 091 17 192 . 16 45 L 10 717 ; 7 269 ! 5 763 5 000 ; 2 700 2 ООО i 700 i
* Под названием действительные обозначены залежи, полностью изученные; вероятные -залежи, дгишь частично исследованные, и возможные -залежи, о которых известно лишь их местоположение. При этом необходимо отметить, что в подсчет вошли запасу до глубины 1 ООО м, содержащие не менее 35% серы. ЙЗ бед-лых серой колчеданов (28-30% S) включены лишь те, к-рые выгодно обогащать. далеко от потреб.чяющих центров, из которых многие, например Украина, совершенно лишены пиритовых месторождетй. Благодаря этому возник вопрос о замене П. при производстве серной кислоты другими материалами; так, Ин-том прикладной минералогии были поставлены успешные опыты получения серной к-ты из ватержакетных газов, отходящих при сжигании медных колчеданов на медеплавильных заводах Урала и др. П., содержащие золото в количествах, допускающих выгодность его извлечения; а также медь и кобальт, разрабатываются, кшг руды этих металлов; П., содержащие сечен' и теллур, применяются в стекольном и дру- гих производствах, а также в воепно-химич. деле для изготовления газов-диэтилтеллу-рита и диэти л селенита. Лит.: Будников П.П., Химическая технология минеральных веществ, Иваново-Вознесенск, 1927; - 3 а м я т и н П. М., Богомоловское дело с точки зрения возможностей снабжения проектируемого завода минеральным сырьем, Уральский техник , Свердловск, 1927, iO; 3 а м я т и н П. М., Колчеданные месторождения района Богомоловских рудников на Урале, МС , 1927, 5-6; Захаров Е. Е., Первичные полосатые структуры колчеданных руд восточного склона Урала, Труды Ин-та прикл. минер, и цветной металлургии . Л., 1927, вып. 32; Кусов В., Серный колчедан Подмосковного бассейна, Бумажная промышленность , М., 1926, 2-3; Меншуткин Б. иВольф М., о действии дымящей серной к-ты на циклогексан, НХ , 1927, 9; Мурашов Д. Ф., о составе богомольской руды, Вестн. Геол. ком. , Л., 1927, б; Наумов Я.Я., Предварительные итоги производственной деятельности основной химической промышленности за 1926/27 операционный год, ЖХП , 1927, ii; П а ф ф е н г о л ь ц К. П., Чи-раги-Дзор, месторождение серного колчедана в Ганд-жинском уезде АзССР, Матер, по общ.иприкл.геол. , Л., 1928, вып. 102; Самойлов Я., Серный колчедан, Сборник Естественные производительные силы России , П., 1920, т. 4, i9; Федоровский Н. М., Минералы в промышленности и сельском хозяйстве, 2 изд.. Л., 1927; Ферсман А. иЩер-баков Д., Колчедан серный, Хим.-технич. справочник , ч. 1, П., 1923, 1; Юшкевич Н. Ф., Обследование газов ватержакетных печей Калатинского медеплавильного з-да, МС , 1928, 1; Bacon R., Sulplnu- а. Pyrites, Engineering а. Mining Journal Press*, N. Y., 1928, v. 125, 5; D о u g 1 a s G. Т., Note on the Origin of the Rio Tinto Ore Bodies, Economic Geology*, Urbana, 1927, v. 22, 7; Les reserves mondia-les en pyrites, Information faite initiative du Bureau du XIV Congres geologique international*, Madrid, 1926. v. 1-2; Lunge G., Handbuch d. Schwefel-saurefabrikation u. ihre Nebenzweige, 4 Auflage, B. 1, Brschw., 1916; Petersen H., Fortschritte in d. Schwefelsaurelabrikation unter besonderer Berucksich-t igung metallurg. Abgase, Metall u. Erz , Halle a/S., 1927, 18; Truchot P., Les pyrites. P., 1907; Wells A. E., Sulphur, Pyrite a. Sulphuric Acid, Mineral Industry During 1926 , N. Y., 1927. H. Федоровский. ПИРИТОВЫЕ ОГАРКИ (сгарки), отходы, получаемые при обжиге серных колчеданов на предприятиях сернокислотной, бумажной, анилиновой, нефтяной и других отраслей промышленности. П. о. содержат в среднем до 1%Си и до 55% Fe; огарки же медистых колчеданов содержат до 5-6% Си. П. о. в металлургии у нас до сих пор не име-.ли применения; нек-рое количество их экспортировалось главн. обр. в Германию и во Табл. 1 .-А н а л и 8 ы i Францию, значительное нее количество ежегодно погибало на свалках з-дов, в то время как П. о. являются весьма ценным сырьем для получения черных и цветных металлов. В довоенные годы лишь только на одном Константиновском заводе велись опыты по применению П. о. в доменной плавке. В настоящее время на названном заводе имеется небольшая установка для агломерации П. о. в горизонтальной вращающейся печи. За последние годы П. о. стали применять пока еще в незначительных размерах в цементной, лакокрасочной и прочих отраслях промыш ленности СССР. В Германии ежегодно перерабатывают значительное количество П. о. не только местного происхождения, но и импортируемых из Испании, Швеции, Норвегии и СССР, несмотря на накладные расходы по транспортированию; там извлечение из них меди считается рентабельным даже при содержании 0,2% последней. В настоящее время в связи с резким дефицитом черных и цветных металлов перед промышленностью СССР встал вопрос о максимальном использовании П, о. не только в доменном производстве, но и для извлечения из них меди, для чего в Московской и Ленинградской областях намечается организация чугунолитейных комбинатов с доменным хозяйством для переработки агломератов из П. о. Такие же установки проектированы на Днепровском и других комбинатах. В настоящее время получено специальное оборудование из Англии и Америки для установки работы с П. о. в полузаводском масштабе и уточнения технологич. процесса. Перспективы получения этого вида сырья для черной и цветной металлургии чрезвычайно значительны в виду увеличения производства в СССР серной к-ты, дающего гл. обр. этот вид отбросов. Огромные запасы названного отхода накопились на свалках за минувшие годы; так, по инспекторскому обследованию Металлома предприятий химической промышлениостиустановлено следующее ориентировочное количество этих запасов (в тыс. т): Уральский район-1000, Сев.-иритовых огарков. Наименование заводов Чернореченский Полевений. . . . Бондюжский Пермский . . Кр. Профинтерн . . .... 3-д им. Батурина .... .... Кинешемский...... ...... Константиновский . . . ... Окуновский..........Свеж. Им. Фрунзе . . . . Кр. химик . . . . 3-д б. Морозова . . Краснознаменный Одесский.....
Зап. район-400, Центр.-Промьпплен.-500, Кавказский район-100, Украинский-400, прочив районы-100; всего-2 500 тыс. ш. Анализы свалочных и текущих П. о. представлены в табл. 1- Чрезвычайно большое значение имеет правильная сборка, концентрация и хранение на производственных предприятиях П. о..как находящихся уже на свалках, так и свеже получаемых текущих отходов. П. о. должны концентрироваться на особых отведенных площадках. Стоимость П. о. обусловливается гл. обр. железнодорожными и водными фрахтами; средняя рыночная цена их составляет 4 р. 50 к. за т. Существующую рыночную стоимость пиритовых огарков расценивают за 1 т, исходя главным образом из подвозки пиритовых огарков к железнодорожным станциям и погрузки их в вагоны или к водным путям и погрузки в баржи. Госпромтрестом Металлом по заданию ВСНХ СССР было поручено профессору В. А. Ва-нюкову разработать методы использования пиритовых огарков в наших условиях. Особенность метода утилизации П. о. проф. Ванюкова заключается в том, что не требуется установки специальных обжиговых печей; обработка П. о. ведется слабым раствором H2SO4. Указанным выше способом на Константиновском заводе удалось извлечь свыше 80% меди от первоначального содержания ее в пиритовых огарках и довести содержание серы до 1,2%, что видно из табл. 2. Схема процесса переработки П. о, представлена нгоке. Заводы по переработке П. о. организуются у самых источников сырья. В настоящее время намечается использование П. о. в первую очередь на з-дах Стали , как уже имеющих агломерационные ф-ки, а также и на тех з-дах, где агломерационные ф-ки будут построены в ближайшее время, а именно: завод им. Фрунзе (ст. Константиновка), завод им. Петровского (Днепропетровск), завод им. Дзержинского (Запорожье), завод им. Томского (Макеевка), Косогорский (Тула), Вьпссунский (Выкса), Кулебакский (Куле-бака). По уральским з-дам Востокостали агломерационные установки имеются на заводах Богословском, КалатинскомиКушвин-ском, и следовательно уральские П. о. по извлечении из них меди смогут быть агломерированы на уральских же металлургических заводах. Выход П. о. как текущий отход от производственных процессов промышленности по данным 33 заводов за третий, решающий год пятилетки по отдельным районам 2.-Состав пиритовых огарков (в %).
ИХ заготовки можно усмотреть из следующих показателей (в т): Уральский район.............55 юо Центральный район........... 148 580 Сев.-Зап. район.............. 76 200 Украинский район............ 119 300 Прочие районы..............26 ООО Всего........ 425 180 Схема переработки пиритовых огарков. Огарки 4- Дезинтегратор Реагент Слабый раствор HgSOi Флотационная машина ЖeлeзняJVIacca Уголь Раствор меди Осашдение цемент, меди Кристаллизатор Серный концентрат в обжиг Смешиватель Агломерация Цементная медь Медный купорос в доменную печь На медный завод Т. Э. т XVI. и Другие два года пятилетки дадут выход П. о. в 1932 г. примерно 790 ООО, а в 1933 г.- 1 200 ООО т, с средним %-ным содержанием 0,7-0,75% Си и не менее 55% Fe, что составит в последние три года пятилетки: 1931 г......... 233 600 железа и 2 975 меди 1932 г......... 440 ООО 5 600 1933 г.........660 ООО 8 400 Приведенные цифры (по данным Метал-лома ) дают ориентировочное количество металла в т. Лит.: Водовозов М. X., Новый источник металла-сырья (Пиритоогарки), Металл , М., 1931, /; ег о же. Отходы и отбросы-мощная сырьевая база металлопромышленности, Металлист , М., 1930, 27;Бельгов В.иДистлер А., На свалках лежит 10 млн. т железа и 100 тыс. т меди, Торгово-промышленная газета , М., 1930, шонь; Шмелев, Использовать колчеданные огарки можно и нужно; чугун, медь и цинк гибнут в отвалах, Новая техника , Москва, 1931, 22; В и д и щ е в С, За медистый металл, там же, 25; Металлом, Доклад Президиуму ВСНХ СССР о пиритовых огарках, М., 1931. Г. Валк. ПИРОГАЛЛОЛ, пирогалловая к-та, триоксибензол, СбНз(ОН)з (1,2,3), трехатомный фенол, изомер флороглюцина (1, 3, 5) и оксигидрохинона (1, 2, 4). См. Фенолы. Впервые П. был получен Шееле в 1786 г. в галловой к-те (см.); кристаллизуется в виде .легких белоснежных кристаллов, легко возгоняется и перегоняется (при 730 мм Hg давления и t° 292-294°) не без разложения; Гпл. 132,5°, уд. в. 1,453; растворим в воде, менее в спирте и эфире. Щелочные растворы П. легко окисляются на воздухе (частица П. поглощает из воздуха 3 атома кислорода и более), принимая при этом коричневую окраску. Многие реакции окисления П, сопровождаются вьвделением света: при действии перекиси водорода (30 %-ной) в присутствии поташа вьвделяется розовый свет, при окислении хромовыми и железными солями в присутствии серебра - белый свет. П. восстанавливает золото, серебро и ртуть из их солей, ядовит. Для П. характерны следующие цветные реахедии: с солями закиси железа он дает белую муть; в присутствии солей окиси железа получается голубое окрашивание, быстро переходящее в коричнево-красное. Нагревание серной к-той с незначительным количеством винной к-ты дает фиолетовое окрашивание. Указанные цветные реакции служат для качественного определения П.; для этой цели служит также нагревание П. с фталевым ангидридом и с избытком серной к-ты, причем П. переводится в 1,2,3-триоксиантрахинон, дающий характерный спектр. Количественное определение П. производят окислением П. раствором перманганата и дальнейшей обработкой йодистым калием, причем вьщеляю-щийся иод титруют тиосульфатом. В природе П. встречается как существенная часть многих естественных красителей (гематоксилин, эллаговая к-та); его диметиловый эфир, СбНз(ОСНз)2(ОН), входит в состав креозота (см.). Синтетически его получают из 2,6-ди-хлорфенол-4-сульфокислоты, к-рую нагреванием с едким кали (до 150-160°) переводят в пирогаллол-5-сульфокислоту, и затем при нагревании с минеральной к-той отщепляется сульфогруппа. Более распространен способ получения П. из галловой к-ты нагреванием с глицерином илис поварепной солью (при 250° и 10 .Ч.Л1 давления) или с водой (при 200-210°). В последнем случае галловую кислоту нагревают с половинным (по весу) количеством воды в автоклаве при давлении 12 atm я при t° 175°; пары воды и углекислоту отводят в холодильник. Процесс длится ок. 3 ч., после чего нагревание прекращают, уменьшают давление и осветляют охлажденный раствор костяным углем. Жидкий П. переливают в плоский железный сосуд, где он остывает. Дальнейшая обработка (путем возгонки или дистилляции) зависит от цели применения П.; для медицинских и фотографических, где требуется П. меньшего уд. в., применяют возгонку. Главное применение находит П. вследствие его восстановительных свойств в фотографии как энергичный проявитель (для негативов и диапозитивов) как в чистом виде, так и в виде смешанных препаратов (см- Проявители). В крашении применяют П. для приготовления некоторых (гл. обр. протравных) азокрасителей (церулеин, галлеин), б. ч. применяемых в крашении мехов; также применяют П. для окраски волос в коричневый цвет, а в комбинации с щелочными солями серебра-в черный. При лечении кожных болезней (псориазис) и сифилиса применяют ацетаты П.: моноацетат- эвгаллол, триацетат - ленигаллол и сравнительно реже употребляемый диаце-тат-с алигаллол.Из производных П. наиболее важное-сульфокислота Cg Н 2(0 Н) gS О gH, получаемая нагреванием П. (25 ч.) с конц. серной к-той (15 ч.) на водяной бане; применяется для окраски волос в черный цвет. Лит.: Энглиш Э., Основы фотографии, пер. с нем., М.-Л., 1927; Ullm. Enz., В. 9. Н. Ельцина. ПИРОГЕНЕТИЧЕСКИЕ ПРОЦЕССЫ, п ир.о генные процессы, пиролиз, пирогенизация, пирогенез, в широком смысле слова химич. превращения, происходящие под влиянием высокой темп-ры и заключающиеся в превращении исходного вещества в другие (без обязательного химич. воздействия посторонних реагентов). Физико-химич. смысл этих превращений заключается в том, что при сообщении телу тепла происходит накопление энергии в молекулах, которые согласно закону распределения Максвелла приобретают способность к изомеризации или разрыву с отщеплением от-дельньгх частей и превращаются в более простые молекулы, обычно более устойчивые при высоких темп-р ах. Наибольшее технич. значение имеют П. п., связанные с органическими веществами естествен, происхождения. Вследствие сложности происходящих при этом химич, процессов до самого последнего времени многое являлось еще далеко не исследованным, и применение этих процессов основывалось гл. обр. на эмпирич. данных; только в самое последнее время создается более твердая научная база для понимания этих важнейших промьппленных процессов. Основными типами П. п, в технике являются: 1) Коксование (см.) каменных углей- термич, обработка их при весьма высоких темп-рах (900-1 250°), связанная с весьма глубокими изменениями исходного вещества и одновременно с образованием больших количеств наиболее простых молекул в виде газов. 2) Швелевание (см.)-низкотемпературная сухая перегонка каменных и бурых углей, горючих сланцев и других битуминозных пород. Характерной особенностью этих процессов является применение более низких темп-р (450-500°) с целью избежать глубокого распада углеводородных продуктов, являющихся смазочными материалами и жидким автомоторным топливом как замена наиболее ценного горючего-бензинов и керосинов нефт. происхождения. 3) Сухая перегонка дерева, см. Дерево, сухая перегонка. 4) Пирогенетич. разложение нефти нее продуктов наряду с коксованием углей является одним из наиболее важных в технич. и хозяйственном отнощении технологич. процессов. Пирогенетич. разложение нефтяных продуктов по своей целевой установке м. б. разделено на 2 основньпс группы: а) ароматизация, высокотемпературный процесс (600-700°), имеющий целью получение низших ароматич. углеводородов, гл. обр. бензола и толуола, и б) крекинг-процесс (см.), П. п., протекающий при более низких темп-рах (425-500°), ведущий к образованию автомоторного топлива: бензинов и керосинов. 5) Деструктивная гидрогенизация, или крекинг в присутствии водорода, с формальной точки зрения можно не относить к П. п., так как участив в процессе водорода в качестве химич. агента выделяет ее среди типичных П. п. Однако по характеру процесса деструктивную гидрогенизацию можно считать в значительной .мере аналогичной обычному крекингу. Химизм пирогенетических процессов. Основньпйи процессами, имеющими место при нагревании органич. веществ до высоких f°, являются: 1) термич. расщепление (дезагрегация); 2) полимеризация и уплотнение и 3) дегидрирование и гидрогенизация. Рассмотрим химизм в отношении отдельных классов углеводородов, заслуживающих с практической точки зрения наибольшего внимания. 1) Метановые углеводороды. Основной реакцией термич. превращения насыщенных алифатич. углеводородов является указанный еще Вертело щ распад по схеме Ст+пНа(ш+п.)+2 СхаНгт+г + СпНга с образованием молекул метанового углеводорода и олефина. Относительно места разрыва цепи и влияния темп-ры, давления и др. достаточно обоснованной теории еще нет. Экспериментальные наблюдения, каса-юпщеся например влияния повьппенного давления на характер разрыва цепи, скорее всего могут быть объяснены температурным релшмом крекинга в жидкой фазе, когда продукты разложения не подвергаются столь глубокому распаду, как это имеет место при процессе в паровой фазе, всегда сопроволс-дающемся явлениями значительного перегрева и потому обусловливающем более глубокое дробление молекул. Именно этим м. б. объяснено значительное образование газов при П. п. под атмосферным давлением. Однако если нормальные углеводороды склонны при первичном расщеплении распадаться по приведенной выше схеме, то молекулы с разветвленньпии цепями могут отщеплять в зависимости от структуры скелета также и преимущественно короткие осколки цепей или даже водород. Поэтому количество обра- зующегося газа при технич. пирогенизации в значительной мере зависит от характера исходного материала. В зависимости от температуры и времени пребывания в реакционной зоне степень дезагрегации исходного продукта меняется и может достигнуть при достаточной темп-ре (вьппе 1 000°) полного распада на элементы. С увеличением молекулярного веса термическая стабильность метановых углеводородов понижается. В метановых углеводородах нормальной структуры происходит также отщепление водорода. :1ри наличии же изостроения дегидрогенизация получает более важное значение; так, при пиролизе изобутана до 50 % его превращается в изобутилен {] по схеме: (СНз)2СН-СНэ (СНз)аС : CHa + Hg. 2) Непредельные углеводороды жирного ряда. Содержащие этиленовые или ацетиленовые связи углеводородные молекулы распадаются аналогично метановым углеводородам, по схеме напр.: С(ш+п)Н2<т+п) СтН2пи2+СиН2д 2, С образованием насыщенного углеводорода и еще более непредельного (напр. с двумя этиленовыми связями). Точно так же возможны реакции отщепления водорода; напр. этилен при 800° дает до 3,5% ацетилена. Имеют место при высоких темп-рах также реакции изомеризации: осколок нормальной цепи приобретает изостроение. Однако наиболее характерньши реакциями олефинов, а также ацетиленовых углеводородов при П. п. являются полимеризация и уплотнение. Работы Доу, Ипатьева [3J и др. показали способность этилена и его гомологов давать циклич. соединения-нафтены, к-рые являются более устойчивыми при высоких темп-рах, по схеме: 3 СНо : СНг СНг НаС/ЧСНа НаСЧУСНа СНг Кроме ТОГО при это.м возможны реакции уплотнения олефинов с образованием более высокомолекулярных ненасыщенных углеводородов; например амилен дает полимеры: ДИ-, три- и тетраамилены. Все эти реакции уплотнения хорошо протекаютужепри400- 450°, а в присутствии некоторых катализаторов, напр. фтористого бора, идут уже на холоду. С увеличением молекулярного веса, оле-фины становятся менее устойчивыми в отношении темп-ры и приобретают большую склонность к реакциям уплотнения. Особенную способность к образованию высших полимеров имеют диэтиленовые углеводороды: эритрен, изопрен и др. Продукты полимеризации этих углеводородов, полученные при низкой темп-ре в присутствии специальных катализаторов, дают искусственный каучук. Из числа многих предложенных методов получения диолефинов наибольшие перспективы имеют пути, лежащие через П. п. Так, для этого может быть использовано разложение при темп-рах 500-700° нефтяных продуктов [ ] или термич. разложение спиртов [6] или конденсация при 350-450° этилена с ацетиленом []; последние м. б. получены также пирогенетически, и т. д. *и 3) Кольчатые углеводороды ряда нафтенов. Близкие по своим химическим свойствам к метановым углеводородам насыщенные нафтены в условиях П. п. более устойчивы. Реакции расщепления идут прежде всего в сторону отрыва боковых цепей, причем легче всего отрываются наиболее длинные цепи, а наиболее устойчива метиль-ная группа. По лиметиленовое кольцо способно также разрываться при высокой темп-ре с образованием ненасыщенного углеводорода с открытой цепью, напр: СНа-СНг I I СНзСН2СН:СНа СНа-СНа К реакциям уплотнения насыщенные циклические углеводороды, как и метановые, мало способны. Весьма своеобразны реакции изомеризации полиметиленовых углеводородов, заключающиеся в изменении числа членов кольца. Так, шестичленные кольца при повышенных темп-рах могут переходить в пя-тичленные [ ] по схеме: СНа СНа СНа СНа \/ СНа СНг СНа CHs СНСНз СНг Аналогично переходят в шестичленные кольца семи- и восьмичленные и т. д. Своеобразной реакцией шестичленных нафтенов является обратимая реакция дегидрогенизации, которая приводит к образованию аро-гатич. углеводородов по схеме: НгСГ НаС СНа СНа Нафтены, не имеющие шестичленного кольца, не способны к этой реакции, что м. б. полонадно в основу метода анализа (по Зелинскому) [8], Однако процессы полимеризации олефинов, а также изомеризация нафтенов могут при П, п, увеличивать количество шестичленных циклов по сравнению с имевшимися в исходном продукте, а последние могут вследствие дегидрогенизации превращаться в ароматические углеводороды. Именно этим реакциям следует приписать самую сущность технологич. процесса ароматизации нефти, имеющей целью получение низших бензольных углеводородов (преимущественно бензола и толуола) из нефтяных продуктов. В результате дегидрогенизации могут образоваться также ненасыщенные циклич. углеводороды, обладающие подобно олефинам сильной способностью к уплотнению, к-рое может привести иногда также к ароматич. углеводородам; напр, Вегер при пропускании через нагретую трубку цикло-пентадиена получил значительные количества нафталина, образование к-рого можно представить по схеме:  НС СН Процессы превращения нафтеновых колец при П. п. довольно хорошо согласуются с теорией напряжения Байера [], согласно которой наиболее устойчивыми д, б. пяти- и шестичленные циклы. 4) Ароматические углеводород ы являются наиболее стойкими. При не очень высоких темп-рах бензольное ядро почти не способно разрушаться, и расщепление идет преимущественно в боковых пенях, которые в отношении термич, устойчивости приближаются к цепям алифатич. углеводородов. Наиболее прочньвии являются короткие цепи: в частности метильная группа отщепляется от ядра при t° выше 700°, Так, Egloff и Moore [ ], изучая крекинг в паровой фазе фракции ароматич. углеводородов, кипящих при 135-170°, нашли, что образование бензола совершенно не имеет места до 500° и начинается при значительно более высоких темн-рах; максимум образования толуола наблюдался при 750°, бензола при 800°. Наиболее характерными реакциями ароматич. углеводородов при П, п. являются превращения, связанные с уплотнением молекул. Реакции конденсации можно разбить на два следуюпщх основных типа: 1) уплотнение ядер между собой по схеме 2СвНв->-СбН8СбН5 + Н2 и 2) уплотнение молекул за счет ненасыщенных соединений, присутствующих в смеси с ароматическими, или за счет непредельного характера цепей у бензольного ядра. Реакция уплотнения I типа, т. е. за счет подвижности водорода в бензольном ядре, весьма распространена в П. п. при высоких темп-рах; в отношении бифенила пирогенизация является даже способом его получения Аналогично осуществляются реакции образования динафтила из нафталина, бифенилбензола из бифенила с бензолом; динафтил ведет к образованию пирена, а также перилена [] по схеме:  Близкими по механизму являются реакции соединения ядер при посредстве простейших боковых цепей, например при нагревании до красного каления толуола идет образование антрацена. Бэр и Дорп получили из о-бензилтолуола также антрацен, что указывает на вероятность его роли в этом процессе как промежуточного продукта. Характерной особенностью приведенных реакций первой группы является сравнительно высокая темп-ра, необходимая для уплотнения, так как большинство представителей ароматич. углеводородов, не заключающих в боковой цепи этиленовой связи, не изменяются при t° в 450-500° [ ]. Несколько иной характер имеют реакции уплотнения, идущие за счет ненасьппенных углеводородов, К таковым могут быть отнесены синтезы Berth [18], приводившие к образованию многокольчатых углеводородов при нагревании бензола и его гомологов с этиленом и ацетиленом. При нагревании этилена с бифенилом происходит образование фенан- 1 ... 18 19 20 21 22 23 24 ... 48 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
© 2007 SALROS.RU
ПромСтройМат |