 |
 |
 |
 |
1 ... 15 16 17 18 19 20 21 ... 48 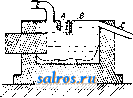 Фиг. 2. ворят в пользу этого способа. Однако несмотря на весьма большое количество взятых патентов этот способ все еще не получил скслько-нибудь значительного практич. применения. Причшюй является трудность конструирования аннаратуры, стойкой при высоких t° по отноше1П1ю к хлору и натрию. Кроме того весьма неблагоприятными факторами являются: близость t°m NaCl (800°) к t\ . Н. (877,5°), малый уд. в.метал-ла и его крайне легкая окисляемость. Одно из наиболее удачных выполнений этого способа принадлежит Акционерному обществу .Понца в Базеле. Ванна, предлслоенная этой фирмой, изображена схематически на фиг. 2; в плане она и.меет вид прямоугольника; футеровка внутри nainibi выполнена из огнеупорного кирпича; аноды D, состоящие из особого сорта угля, в виде пластин расположены горизонтально; катод представляет собою железную коробку В, закрытую сверху и снабженную боковой сливной трубой С. Над анодами расположена шамотная крышка, погрулсенная своей закраиной в электролит; под крышкой собирается выделяющийся на аноде хлор, откуда по трубе Е он отводится в соответствуюпцге приемники. Анодное и катодное пространства разделены друг от друга при помощи диафрагмы А-стенки, сделанной из изолирующего материала (циркон, корунд и т. п.), к-рую прикладывают к обращенной в сторону анода стенке катода. Вследствие отклонений линий тока, в месте соприкосновения электролит охлаждается и застывает, связывая так. обр. стенку-диафрагму с катодом. Натрий выделяется на внутренних стенках катода и по мере иовыитения уровня под последним сливается через трубку С. Степка А в случае необходргмости легко м. б. во время работы вынута и заменена новой. В остальном устройство ванны от.личается простотой, вследствие чего она может месяцами работать, не требуя ремонта. С они-санной ванной сходен электролизер Данне-еля, в котором составленный из отдельных угольных пластин анод располагается вертикально. В аппаратах подобного устройства возможно работать с выходом по току до 75%. Амперная нагрузка отдельной ванны достигает 4000 А, напряжение в среднем 18 V. Удельный расход энергии определяется в 27 kWh на 1 кг Н. Мировое производство Н. в 1929 г. составляло 25 ООО т при средней цене в Германии 2 250 мар. за т. З-ды имеются в Германии, Франции, Швейцарии, Англии, Норвегии и США. Главнейшими применениями металлич. Н. являются приготовление перекиси Н. и цианистых соединений. Лит.: Федотьев П., Электрометаллургия, т. 2, Ленинград, 1923; Becker Н., Die Electrometallur-gie d. AlkaHmetalle, Monographien iiber angewandte Electrocliemie, B. 9, Halle a/S., 1903; В i 11 i t e г J., Technische Electrocliemie, Die electrocheraischen Ver-lahren der chemischcH Gross-Industrie, B. 3, Halle a/S., 191U; Regelsberger F.. Chemisdie Technolo-gie d. Leichtmetalle u. ihrer Legierungen, Lpz., 1926 (bo всех этих трудах обширные ссылки на журн. статьи и патентную литературу). П. Антипин. НАТРИЯ СОЕДИНЕНИЯ. Достоверно известны лишь соединения одновалентного Na. Во всех Н. с. атомы Na проявляют резко металлический характер; они образуют только один вид ионов-бесцветный однозарядный катион Na , не осаждаемый сероводородом; в составе комплексных ионов Na не встречается. Для Na известен непрочный гидрид NaH и весьма прочная окись NagO, гидрат которой, NaOH, в растворах сильно ионизирован и об.ладает свойствами энергичного основания (едкая щелочь). Все соли Na хорошо растворимы в воде; иск.лючения из этого правила весьма редки и наб.людают-ся .лишь для немногих солей с тялселыми и сложнььми анионами (см. ниже - Анали-тич. определение Na). Из растворов соли Na кристаллизуются б. ч. в хорошо образованных, богатых водою кристал.логидратных формах. Все природные Н. с. представляют собою натриевые соли раз.личных к-т-гл. обр. хлорид, флюорид, нитрат, су.льфаты, карбонаты, силикаты, фосфаты, арсенаты и бораты; помимо земной коры и водных бассейнов соли Na встречаются во всех животных и растительных организмах. Гидрид натрия, водородистый натрий, NaH,-бесцветные кристаллы, уд. веса 1,40. Получается нагреванием металлического Na в струе водорода при 300 - 360° и быстрым охлаждением возгоняющихся паров NaH. Кристаллы при температуре выше 400° диссоциируют ио.лностыо на водород и Na. Ня воздухе NaH быстро окисляется; с водою NaH бурно реагирует по уравнению NaH-f HgONaOH + Ha; во влажной атмосфере эта реакция иногда сонровонсдается воспламенением. С газообразным аммиаком NaH образует амид натрия; COg восстанавливает до свободного углерода; с SO а дает гидросульфит, по ур-ию: 2NaH + 2S02 = Na2So04+Н2. Окись натрия, NagO,-гигроскопич. масса белого цвета, уд. веса 2,3; плавится в краснока.лильном жаре. Способы получения: 1) сплав.лением перекиси натрия с металлич. натрием: NagOg + 2Na= 2Na20; 2) окислением расплавленного Na (нри t° 250-300°) селитрой или нитритом: 10 Na +-2NaN03 = = eNagO+Na; 6Na+2NaN02 = 4Na20+N2; 3) действием окиси углерода па NaCl при высокой темп-ре: 2NaCl + со = NaaO + Clg + С. Все эти реакции долями ы проводиться без доступа воздуха. С водой NagO моментально образует NaOH и мол-сет слулсить как энергичное водоотнимающее средство. Имеется ряд попыток использовать NagO в качестве конденсирующего агента цри технич. синте-зах.Перекись натрия, NagOg,--желтовато-белого цвета, в расплавленном состоянии- оранжевого; образуется нри сжигании Na в кислороде; уд. в. 2,5; Г„.>320°. О технич. получении и применении см. Перекиси. Кроме указанных двух окислов Na- нормального и перекисного тина-существует еще трехокись состава NagOg, розового цвета, образующаяся при пропускании кислорода в раствор Na в жидком аммиаке. Гидрат 0КИСР1 натрия, NaOH,- см. Едкий натр. Натронная или и а т -ристая известь - тесная смесь NaOH и Са(0Н)2, выпускаемая в продажу в виде пористых кусков или зерен. Ее получают, обливая негашеную известь конц. раствором NaOH: за счет раствора известь гасится, причем вся масса вспучивается и затвердевает; для удаления остатков воды ее подвергают умерегиюму прокаливанию. Применяется для сушения и очистки газов. Амид натрия, NaNHg, - полупрозрачная лучистокристаллич. масса, в чистом виде беспветная, обычно же окрашенная в зеленоватый цвет; 210°; при более высокой t° улетучивается; ири 500° разлагается на элементы, частично же переходит в нитрид натрия, NagN (черный порошок). Амид натрия химически весьма активен: с водой он образует NaOH и NHg, с хлористым водородом-NaCl и NHCl, с окисью углерода NaCN и НаО, с СО. при нагревании- цианамид и воду и т. д. Растворяется в жидком аммиаке; при сплав.чении с Na не изменяется. Технически NaNHg получают пропусканием чистого сухого аммиака в расплавленный натрий при t° 300-400°. NaNHg применяется в органич. синтезе для амини-рования, например для получения аминосо-единений из фенолов, нафтолов и ароматич. сульфокислот; он используется также как конденсируюшее средство в ряде синтезов (напр. в синтезе индиго по Гейману), служит для получения азида натрия (см. ниже) и т д. Возможности применения NaNH в органич. реакциях весьма обширны и разнообразны. Цианамид натрия, NagCNj, - см. Цианамид. Цианистый натрий, NaCN, - см. Цианистые соединтия. Азид натрия, NaNg, соль азотисто-водородной кислоты,-гексагональные кристаллы, уд. в. 1,48; при нагревании и ударе си.?1ьно взрывает. Хорошо растворим в воде (40,5:100 нри 15°), плохо-в спирте(0,3:100), нерастворим в эфире. Технически получается: 1) пропусканием хорошо высушенной закиси азота над расплавленным амидом натрия при t° ок. 190°: NaNHa + NaONaNa+HaO, ИЛИ 2) кипячением гидрата гидразина с амил-нитритом (N0 ОСдНц) и едкой щелочью в спиртовом растворе. Азид нат]ия слулшт для получения азида свинца, к-рый употребляется как инициирующее взрывчатое вещество. Сульфид натрия, NaaS-xHgO (где х=0,1,41/2,5, 51/2. 0,9,10),-см. Сернистый на-тргш. П о ли с у л ьфиды натрия различного состава содержатся в технич м н о-госерн истом натрии. Из представителей этого ряда известны: дисульфид Na2S2,тpиcyльфид NaSs.TeTpaсульфид NaSi и пентасульфид Na2S5,H3 них наиболее устойчив Na2S4. Многосернистый натрий (смесь полисульфидов) - желтая или коричневая твердая масса; для его получения вносят порошок серы в расплавленный кристал.чич. сернистый натрий (NajS-O HgO) и нагревают до растворения при 100 , затем выпарршают досуха; продукт содержит переменные количества S и HgO. Пентасульфид может быть получен также прокаливанием гипосульфита. Многосернистый натрий применяется при фабрикации сернистых красителей и в борьбе с вредителями виноградников. Г и д-росульфид натрия, сульфгидрат натрия, NaSn,-в безводном виде р-1меет Г„д. около 350°; ири нагревании до 500° разлагается naNajS и H-iS; легко растворим в воде, растворяется в метиловом и этиловом спиртах; сильно гигроскопичен; образует гидраты с 3, 2 и 2 молекулами П^О (обычная форма - NaS 11 2 Н2О). Полутается путем насыщения раствора Na.S (либо NaOH) газообразным сероводородом: Na.-S + H.S = 2NaSH. Технич. продукт содержит примесь Na2S. NagSOs и NaSaO;,. Применяется непосредственно в виде водного раствора и служит гл. обр. для денитрации волокна в производстве нитроцел.люлозного искусственного шелка. Фтористый натрий, флюорид натрия, NaF,-кристаллы уд. в. 2,8; ок. 990°, f° . 1 695°. В природной форме представляет минерал вильомит; более распространены технически важные двойные флюо-риды Na и А1-к р и о л и т, AIF3 3 NaF, и X иол ИТ, ЗА1з-5 NaF. О производстве и применении NaF см. Фтора соединения. Хлористый натрий, NaCl,-см.Ло-варенная соль. Бром истый и атрий, NaBr,-см. Брома соединения. Йодистый натрий, NaJ,-см. Иода соединения. Гипохлорит натрия, хлорновати-стокислый натрий, NaCIO, хлорат натрия, хлорноватокислый натрий, NaClO- и перхлорат натрия, хлорнокислый натрий, NaClO*,-см. Хлора соединения. Нитрат натрия, азотнокислый натрий, натриевая селитра, NaNOg, см. Селитра . Нитрит натрия, азотистокислый натрий, NaNOa, ромбические призмы, уд. веса 2,17, 1°пл. 271°. Растворимость в воде 83,3 : 100 при 15°; реакция растворов слабо щелочная. При действии кислот выделяет бурые пары окислов азота (в разбавленных растворах получается свободная азотистая кислота HNOo). Нитрит легко образуется при действии различных восстановителе[ на нитрат NaNOg; этот путь долгое время применялся и для технич. получения нитрита. В данное время нитрит вырабатывается исключительно из нитрозных газов, по.лу-чаемых при дуговом методе фиксации атмосферного азота или при контактном окислении аммиака. Нитрозные газы по выходе из печи подвергают охлаждению и поглощают раствором едкого натра: NO + N02+2NaOH=2NaN02+H20. Обычно нитрит получают как побочный продукт при производстве азотной к-ты или нитратов, используя для этой цели остаточные нитрозные газы, отходящие из абсорбционных установок. Для поглощения окислов азота нередко вместо NaOH применяют раствор соды. Нитрит применяется в больших количествах для реакций диазотиро-вания,-гл. обр. при производстве органич. красителей; в последнее время его начали также применять для консервирования мяса. П е р м а н г а н а т натрия, NaMnOi,- см. Марганца соединения. Сульфат натрия, сернокислый натрий, КааЗОд. Безводная соль полиморфна. имеет уд, вес 2,67-2,70; ее t° и t° 1 430°; о производстве и применении см. Сульфат. Водная форма, NajSOj-lO HgO,- см. Глауберова со.чь. Минералогии, формы, в виде к-рых NaaSOi выкристаллизовывается из природных соляных бассейнов, довольно многочисленны; они представляют собою простые или двойные сульфаты, например: тенардит Na.SOi,мирабилит NajSOi-10 HgO, дараискит Na..S04-NaN03-HgO, глазерит NaKaCS О4) 2, астраханит Na .S O4 MgS O4 4 HjO, лёвеит 2 Na2S04-2 MaS04-5 HoO, вантгоффит 3Na2S04-MgS04, глауберит Na2S04-CaSOj, ферринатрит 3 Na2804-Ре 2(804)3, натроалу-нит NaAKSOiCg-AlgOa-S HgO и др. Бисульфат натрия, NaHSOi, кристаллы триклинной системы, уд. веса .2,74, легко растворимые в воде; реакция растворов сильно кислая; из раствора при температуре ниже 50° кристаллизуется в форме NaHS04- HgO, моноклин, системы. Получается как побочный продукт при производстве -азотной ш1слот.ы (см.) из селитры; в этом виде он содерлсит значительные количества среднего сульфата Na2S04 и ииросульфата Na.SaO а также примесь солей Fe, А1, Са if Mg. Чистый бису.льфат готовится нагреванием NaSOi с избытком серной кислоты и кристаллизацией из небо.льшого количества воды. Бисульфат является малоценным про--Дуктом: при ограниченности его применения и массовой выработке, он иногда не использовался целиком и выбрасывался без утилизации. Прялюе применение бисульфат находит в производстве фосфорнокислых удобрений, уксусной и высших жирных кислот, искусственного (вискозного) шелка, гипсового цемента, в колсевенном деле, для*травления метал.лов,регенерации каучука и т. д., заменяя в этих случаях H2SO4; он перерабатывается также на средний сульфат и сво- бодную H.S04 либо на сульфат аммония. Натриевые к в а с ц bi,NaAl(S04)2- 12 Н 2О,-см. Квасцы. С у ,л ь ф и т натрия, сернистокислый натрий NagSOa и бисульфит натрия NaHSOg, см. Сульфиты. Гипосульфит натри n.NaoSgOs- 5 HgO,-см. Гипосульфит. Гидросульфит натрия, Na2S204, и с у л ь ф о к с и .л а т натрия, NaHS02, см. Гидросульфит. Персульфат натрия, надсерно-кислый натрий, NaaSgOg,-см. Нерекиси. Хромат и б и X р о м а т натрия, NagCrOi и NagCrgOy,-см. Хрома соединения. Карбоиат и бикарбонат натрия, NagCOg и NaHCOg,-cai. Сода двууглекислая. Перкарбонат натрия, надуглекис-..лый натрий, Na2C04,-см. Нерекиси. С и л и к а т ы н а т р и я. В природе рас-пространень[ сложные Na-coдepж;aщиe си--ликаты, напр. нефе .л и и, NaAlSi04, я ад е и т или г .л а у к о ф а и, NaAl(Si03)2, альбит, NaAlSiaOg, цео.литы (натролит, анальцил!) и др. Пскусственно получаемый метасиликат натр[ьч Хд.,810з-см. Растворимое ствк.яо. т. Э. т. XIV. Фосфаты натрия. Многочисленные природные фосфаты содержат Na наряду с Са, А1, Ми или Be. Из искусственно получаемых фосфатов (см. Фосфора соединения) технич. ирименение имеет двунатри-евый ортофосфат, NagHPOi-12 HgO, кристаллизующийся в монок.линной системе, уд. веса 1,53 и 1°пл. 40°. Растворимость (безводной соли) в воде: при 0°-2,5 ч.. при 100°-ок. 100 ч. в 100 ч. Н2О. Его получают нейтрализацией фосфорной к-ты содой (до слабо щелочной реакции) и затем криста.л-лизуют из раствора, плотность к-рого д. б. ок. 27° В6. Фрсфат натрия применяется в текстильном деле для отяжеления шелка и при крашении, для огнестойкой пропитки тканей, для получения глазурей, при паянии металлов, в технологии брожения как питательный материал д.ля бактериальных ку.ль-тур ИТ. д. Двойной фосфат Na и аммония Na(NH4)HP04-4 Н2О (монок.линные кристаллы удельного веса 1,55, Ь°пл. 9°)-употребительная соль в химич. анализе. Бораты натрия-см. Вора соединения. Перборат натрия, надборпо-кислый натрий, NaBOg,-см. Нерекиси. Формиат натрия, HCOONa, - см. Муравьиная кислота. Ацетат натрия, СНд COONa,-СМ. Уксусная кислота. П а .л ь -.м и т а т, с т е а р а т и о л е а т и а т р и я--см. Мыловарение. Окса.лат натрия, щавелевокислый натрий, Na2C20i,-см. Щавелевая кислота. Аналитическое определение Мав Н. с. А. Качественные реакции.!) Соли Na окрашивают пламя горелки в желтый цвет. 2) Раствор КзНдЗЬгО? дает с солями Na мелкокристаллический осадок кислого (двуметаллич.) нироантимоната Na2H2Sb.307 6 Н.О. .3) Кремнефтористоводородная кислота HaSlFe. дает студегшстый осадок NaaSiFg. 4) Диоксивинная кислота (СО-00011)2 дает на .холоду кристаллический осадок Na-соли. 5) Цинк-уранил-ацетат в водно-сниртовом растворе дает осадок Na-Zn-UOa-aqcTaTa, NaZn(U02)3(CH3-COO)3-6 НаО. 6) Магний-уранил-ацетат в спиртовом растворе или кобальт-уранил-ацетат в разбавленном уксуснокислом растворе дают аналогичные осадки тройных ацетатов желтого цвета. 7) Раствор K-Bi-нитрита в присутствии CsNOa (~1 %) дает желтый осадок тройного нитрита, состава 6 NaNOa 9 CsN02-5Bi(N02)3- См. Микрохгичичесутй анализ. Б. Количественное определение Na. 1) Весовы.м путем: а) в виде хлороплатината натрия NaaPtCle, отделяемого от соответствующего К-со-единения растворением первого в спирте; б) в виде NaCl, после отделения Na от остальных металлов (калий м. б. выделен в виде KBF4); в) в виде суммы сульфатов натрия и калия (после удаления других металлов), определяя в ней общее количество серной кислоты. Если общий вес Na2S04+K2S04 равен ь, а отвечающее ему общее количество H2SO4 равно а, то количество Na2S04 (х) м. б. вычислено по ф-ле: x = 4,41 (1,78 а-6). 2) Объемным путем, по Окатову: осаждают Na в виде соли диоксивинной к-ты, растворяют в HaS04 и титруют органич. анион оксидиметрически, при помощи кмпо4. 3) Колориметрич. путем: осаждают Na в виде Na-Zn-U02-aneTaTa (см. выше), растворяют последний в уксусной кислоте, прибавляют определенное количество K4Fe(CN)6 и колориметрируют по образующемуся красно-бурому окрашиванию раствора. Лит.: Менделеев Д. И., Основы химии, 9 изд., гл. 12 и дополненияк ней,М.-Л., 1928; Ф о к и н Л.Ф., Обзор химич. промышленности в России, ч. 1, гл. 4, п., 1920; G m е 1 1 ns Handbuch d. anorgan. Chemie, 8 АнП., System-Nummer 21 (Natrium), 8 Aufl., В., 1928; E p h r a i m F., Anorganische Chemie, 4 Aufl., Dresden-Lpz., 1929; Ull. Enz., B. 8. B. Янковский. НАУЧНАЯ ОРГАНИЗАЦИЯ ТРУДА (НОТ), базирующаяся на научных основах организация труда, содействующая иовышенгпп производительности труда при создании ол-иов1)емеино наибо.лее б.лагоприятиых ус.Л1)- 1шй труда для работающих. Подобно тому ivaK слово организащтя можно толковать и как действие и как состояние, точно так A<Q, говоря О Н. О. Т., можно иметь в виду . 1ибо действие по постановке труда на науч-1п.1х основах в определенной области либо состояние дела постановки труда в том или в 1п10м конкретном случае. Основополож-тиигом Н. о. т. является американский ишк. Ф. Тейлор (см. Тейлоризм), пололшвший начало scientific management, науке об управ-.тении, как он назвал предложенную имирп-] .ладную дисциплину. Приоритет Тейлора иадлелснт конечно понимать условно, так 1\-ак, являясь представителем капиталистич. строя, Тейлор относился далеко не научно к человеч. фактору в производстве. Первая всероссийская конференция но П. о. т. и производства, созванная в 1921 г. и проходившая под руководством проф. В. Бехте-] ева, в обще?! своей резолюции заявила, что считает неправильным отождествление попятил Научная организация труда с -тейлоризмом в виду того, что последний лгипь в указанной (в резолюции речь шла о рациональном использовании технических средств производства.--И. Б.) части совпадает с принципами действительно научной организации производства, мелсду тем как в нем имеются и ненаучные стороны, сводящиеся гл. образ, к чрезмерному повышению напряженности труда, без учета общего ба-.lanca энергии работающего . Н. о. т., использовав учение Техьлора и внеся в него соответствующие весьма существенные поправки, считает одним из валс-1[ейших своих принципов нормирование работы всех машин и установок, а таклге и труда калгдого рабочего. Методы :)того нормирования с применением фото-г])афии рабочего дня, хронометража и других приемов разбираются в специальной ветви Н. о. т.-техническом нормировании. Нормирование выработки тесно связано тахсже с изучением трудовых движений и их рационализацией, с устранением .лишних движений, замедляющих работу и донолнительно утомляющих работающего. В этой области основоположником разработки вопроса является сотоварищ Тейлора-американский инж. Франк Джильбрет, показавший на ана.лизе работы каменщика, что вместо 18 движений, какие расходовал каменщик на кладку каждого кирпича, можно при научной организации кладки обойтись Р/4 движения на киртга с соответствующим повышением производительности труда и с избавлением каменщика от ])яда излишних и утомительньгх нагибаний. Научнаг организация трудовых движений связана с вопросом надлежащей организации рабочего места и подбора наибо-.тее приспособленного к работе инструмента, что содействует более удобной и более производительной работе. В этой части проблема Н. о. т. смыкается с вопросами из области психофизиологии труда. Важией-ишм иринцином Н.о. т. является также нра-ви.льно ироведенное разде.ление труд а, которое дает возможность каждому работнику сосредоточиться на более частом повторении меньшего числа операций, что со- действует автоматизации работы, накоплению упражняемости и вместе с экономией^ на времени, ранее уходившем на переключение от одной работы к другой и перемену инструментов и приспособлений, в весьма-значительной степенп повышает производительность труда. Большим разделением труда характеризуются технически наиболее совершенные формы организапии производства, как массовое производство, в особенности возникшее на базе последнего непрерывно-поточное производство (см.). Разделение труда в управлении привело к т. н. ф у н к ц и о н а .л ь н о м у у п р а в л е-пию в производстве. Анализируя универсализм функций, присущих обычно мастеру в производстве, Тейлор выдвинул принцип необходимости разделения труда и в области управления, разбив универсальные ф-ии мастера и его помощника мел-еду 8 мастерами: мастером, наб.людающим за установкой работы и следящим за всеми работами до того момента, когда заготовка будет укреплена на станке; мастером, наблюдающим за скоростью работы, за тем, чтобы примепя-.лись надлежащие резцы и наивыгоднейшие скорость, но дача и глубина резания; контролером (браковщик), следящим за качестволт работы; мастером, который заведует ремонтом и наблюдает, чтобы рабочие содер-;кали станки в чистоте и порядке и чтобы соответствующий порядок был около станков, где складываются отдельные заготовки (этот мастер наблюдает и за содержанием ремней и приводов); 4 мастера кроме того., по Тей.лору, должны работать в бюро со следующими функциями: мастер, заведуюиц^й ткрядком и ходом работы, намечает весь ход работ для данной заготовки по мастерской и от станка к станку с тем, чтобы работа возможно скорее бььла закончена; мастер, заведующий состав.лением инструкционных карточек, сообщает в производстве все детали работы; мастер, заведующий онределением-времени и цен, вписывает в инструхсцион-ные карточки все уч<азания о времени и стоимости работы; мастер, заведующий общим порядком в мастерской, является администратором, наблюдаюпщм за порядком и налагающим адмршистративные взыскания в соответствующих случаях. Такое разделение труда мелсду мастерами значительно об-.легчает возможность подбора соответствующих .лиц на каждую из вышеперешгсленных функциона.льных работ, значительно упрощенных сравнительно с работой универсального мастера. Такое разделение труда содействует и лучшему выполнению работы по управлению производством. Разделение труда между административно-технич. персоналом на базе функционального управления является одним из прогрессивных принципов современного управления, знающего сейчас специальные органы функционального управления в производстве, как нанр. технико-нормировочное бюро, п.ланово-рас-иределительное бюро, контрольное бюро бюро рационализации. Н. о. т. тесно связана таклсе с нримене-иием соответствующих систем оплаты труда, которые стимулируют производительность его, В условиях СССР, где социалисти- ческая рационализация выдвинула новые формы организации труда, где на базе со-циалистическ. соревнования родились ударные бригады разных видов, где в ряде мест эти бригады переросли в производственные коммуны, вопрос о системах оплаты труда не потерял все лее своей остроты, и поэтому надлежащие системы премирования должны являться добавочным стимулом к повышению производительности труда для рабочих масс, объединенных в ударные бригады. На 1930/31 г. ВСНХ совместно с ВЦСНС наметили например выделение 50 млн. руб. для премирования (коллективного и индивидуального) ударных з-дов, бригад, цехов и отдельных ударников. Н. о. т. одной из своих составных частех! считает проблему надле-леащего инструктирования работы в производстве, с непрерывным повышением квалификации и с непрерывным обучением и продвилсением рабочих. Практика капиталистической организации труда выдвинула целую систему мероприятий как социально-экономического, так и психологич. порядка, направленных на продвижение более преданных делу ( бизнесу , в Америке) рабочих и основанных на расслоении рабочего класса С'О ставкой на рабочую аристократию. Принципиально иное пололеение в производстве, какое занимает в Советском Союзе рабочий, ;шляющийся не только носителем рабочей силы, но и активным участником организа-1ПШ производства, выдвинуло в практике (оциалистич. строительства новые формы как выдвилеения рабочих на командные постыв производстве, так и переквалификации и обучения путем своеобразной организации заводов-втузов и других форм обучения. К'ак извращение социалистич. П. о. труда необходимо отметить пропагандируемую А. Гастевым реакционную теорию о современном рабочем как о придатке машины , обучение которого должно в основном ограничиться привитием ему рабочих навыков вместо приобщения его к политехнич. образованию. Защищавшаяся Гастевым в течение ряда лет точка зрения в последнее время всесторонне разоблачена как реакционная и ониортунистич. установка, и происходивший в августе 1930 г. Всесоюзный по-.титехнический съезд признал, что взгляды Гастева не отвечают принципам построения политехнич. школы в социалистич. стране. В арсенале Н. о. т. одним из могучих средств, содействующих успешности труда и наибольшей удовлетворенности каждого из его участников, является надлежащее разрешение проблемы подбора персонала для каждой работы. В соответствии < требованиями, какие предъявляет к рабочему та или иная профессия, Н. о. т. методом профессионального подбора выбирает из наличного состава рабочих наиболее подходящих для данной работы лиц. С другой стороны, в соответствии с определенными свойствами данной личности, необходимо ири помощи профконсультации ее правильно профориентировать. При профподборе и профориентации применяются специальные методы пограничной с Н. о. т. области знаний, т. н. психотехники. Н. о. т. требует таклсе при каждой работе-и в этом одна из характернейших ее особенностей-создани я таких условий труда для рабочих, при которых они были бы наиболее целесообразно обслужены с гигиенич. и психофизич. точет; зрения. Здесь имеются в виду определенн1ло требования в отношении t° помещения, влажности воздуха и его ныльности, освещения помещения и его окраски. Опыты по-каза,ли, что от разнообразной окраски помещения, а также и от различной степени ос-вещеппости в большой мере зависят и производительность труда и самочувствие работающих; последние вопросы являются предметом изучения гигиены труда (см.) и псп-хофизиолопш труда. К области изыскани!! последней относятся п такие вопросы Н.о.т., как например организация рабочего места, приспособленного к анатомии, и психофизиологическим требования:*!, как организация соответствующего релшма работы с определенным чередованием времени работы и отдыха, в целях уменьшения утомления и повышения производительности труда. К области широко понимаемой Н.о.т. относятся также такие проблемы, как специализация предприятий и их кооперирование, как организация производства, рационализация (см.), стандартизация (см.) и др. Научной разрабопсой проблем Н. о. т. в СССР занят ряд институтов: Центра.льны{г ин-т труда, Ин-т охраны труда и Ин-т техники управления (Москва), Ин-т рационализации управления (Харьгсов), Казанский ин-т НОТ и ряд институтов в сети Наркомтру-да и Наркомздрава, с задачами разработогс но .линии охраны труда и его оздоровления. Общество работников Н. о. т. (ОРИ) объединяет как общественная научная организация соответствующих специалистов в области П. о, т. Обмену опытом в области Н. о. т. содействуют научные конференции: Первая всероссийская конференция собрана была в 1921 году. Вторая всесоюзная конференция в 1924 г.; в 1925 г. ВСНХ собрал Всесоюзное совещание по рационализации производства; в июне 1930 года ВСНХ сов--AiecTHO с Госпланом и ВЦСПС собрали Всесоюзную конференцию ио рационализации и борьбе с потерями (конференция разбира-.ла в основном организационные вопросы). В 1931 году намечается Третий всесоюзный съезд по рациона.лизации. За границей в ряде стран имеются ин-ты, занимающиеся различными проблемами научной организации труда; наиболее известны: руководимый проф. Атцлером ин-т физиологии труда в Дортмунде, Японский ин-т труда в Кура-шики. В связи с усилением капиталистич. рационализации почти все страны Запада используют в своих це.лях пропаганду научных методов, будто бы .лежащих и в основе капиталистич. рационализации; в связи с этим почти во всех странах организованы с подавляющим участием промышленных II финансовых кругов национальные комитеты по И. о. т. Такие комитеты имеются в Бельгии, Болгарии, Франции, Италии, Го.л-.ландии, Польше и других странах, В Германии и Австрии существуют государственные кураториумы по рациона.лизации. Эти национальные комитеты объединены в ме-ледународно.м комитете по Н. о. т., основной ф-ией которого является созыв международных съездов но Н. о. т. Таких съездов до сих нор было четыре: первый в 1924 г. в Праге (на нем участвовала и советская делегация), второй в 1925 г. в Брюсселе, третий в 1927 г. в Риме, четвертый в 1929 году в Париже. В виду того что организация этих съездов находится фактически в руках капиталистических групп и что рабочая общественность на эти съезды не привлекается, научные учреждения и промышленные предприятия СССР в последние годы на этих съездах не участвуют. Пятый международный съезд по П. о, т. состоится в 1932 г. в Голландии. В качестве международного центра по Н. о. т. с задачами главн. образом информационного и научно-библиографического характера функционирует с 1927 гсда Международн. ин-т НОТ в Женеве; членами этого ин-та являются отдельные институты, предприятия и лица. В виду организационных связей ин-та с Лигой наций советские ученые учреждения не входят в качестве членов в этот ин-т. Лит.: Тейлор Ф., Административно-технич. организация нромышл. предприятий, пер. с англ., Москва, 1918; его же, Научная организация труда, пер. с англ., 2 изд., М., 1924 (две работы Тейлора); Джильбрет Ф., Изучение движений как способ повысить производительность труда, 2 изд., М., 1924; Б у р д я н с к и й И., Основы рационализации производства, Москва, 1930; Труды Первой всероссийской конференции но научной организации труда и производства , вып. 1-6, М., 1921; Тезисы и доклады Второй всесоюзной конференции по научной организации труда и производства, Москва, 1924; Atti del III Congr. Intern, di Organlzzazione scienti-fica del lavoro, Roma, 1927; IV Congrfis International de Iorganisation scientifique du travail, Memoires, Paris, 1922. И. Бурдянский. НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ИНСТИТУТ, см. Организация научных исследований и промыгиленных испытаний. НАФТАЛИН, С^Ня, углеводород ароматического ряда, кристаллизующийся в блестящих бесцветных листочках моноклинич. системы, с характерным запахом; 80°, imm. 218°. Уд. вес твердого Н. = 1,1517, лшдкого-Б^ = 0,9628. В воде Н. практически нерастворим. Растворимость Н. в вес. частях на Юо ч. различных органич. растворителей (при 15°) следующая: Этиловый спирт..................5,29 Бензол (чистый)..................45,80 Толуол ......................32.00 Ксилол.......................Я,50 КуМОЛ.......................30,10 Продажный 90%-ный бензол...........43,20 Сольвент-нафта..................31,72 Смесь из 50% бензола -Ь 50% толуола......39,80 30% + 70% ......37,20 50%-пый продажный бензо.-i...........31,80 Петролейны1£ эфир (уд. вес 0,672)........ 16,90 Креозотовое масло (уд. вес 1,03 с содержанием 8% фенола)...................9,65 Тяжелое масло..................8,90 Нефтяное масло (уд. вес 0,885).......... 11,20 Крезиловая к-та (смесь всех трех крезолов,получаемая при перегонке камен. угля; уд, в. 1,оь9) . 15,20 Упругость паров Н. при различных t°:
.\ш рт. ст. 166,5 222,7 298,8 387,1 495,0 630,8 796,5 1 487,0 Теплота плавления нафталина 35,68 Cal; теплота испарения 75 Cal; теплота сгорания (твердого И.) 9 624 Cal; удельная теплоемкость твердого Н. 0,310, жидкого (при 83°) 0,396. Молекула нафталина содержит 2 конденсированных бензольных ядра (имеющих два общих углеродных атома); ее строение изображают обычно как бициклическое; представление же о пространственном расположении атомов и о распределении валентности стоит в зависимости от того или иного взгляда на строение бензольного ядра. Для обозначения места замещающих групп в Н. пользуются следуюи1ей нумерацией углеродных атомов: или 4 1 /СО. в химическом отношении ядро Н. оа.ла-дает значительной устойчивостью; реакции его являются характерными для ароматич. углеводородов вообще, отличаясь лишь ббльшим разнообразием продуктов замещения но сравнению с бензолом. При окислении нафталина получается фталевый ангидрид Обработка Н. разбавленной азотной кислотой при обыкновенной 1° дает а-мононитронафталин, при нагревании-ди-нитронафталиньцпри действии крепкой азотной к-ты или нитрующей смеси получаются три- и тетранитронафталины, обладающие взрывчатыми свойствами. Крепкая серная кислота при t° до 70° дает а-нафталинсульфо-новую к-ту, а при повышенных t° (~160°)- соответственный )?-изомер, служащий в технике источником для получения у?-замещен-ных нафталина. При продолжительном нагревании Н. с H2SO4 образуются дисульфо-кислоты (см.) нафталина. П. содеряштся в больших количествах в каменноугольной смоле, иногда до 10%, а обычно 5-6%. Джонс установил, что Н. присутствует .лишь в смолах, полученных при 1° выше 750° (так что присутствие Н. в смоле служит признаком, что данная смола- не первичная), хотя Фишер, Шрадер и Зербе указывают, что первичная смола содерлшт некоторые дериваты П., как а- и /З-метпл-нафталины. Смолы, получаемые из горизонтальных и наклонных газовых реторт, содержат Н. примерно в таких же количествах, как и смола из коксовых печей (8-11%). но вертикальные реторты дают пониженный выход Н. Смо.ла водяного газа также содержит Н. до 1,5%; в небольших количествах Н. содержится в смолах доменных газов. Содержание нафталина в светильном газе следующее: темп-ра °С . . . Упругость паров в мм рт. ст. . . Количество Н, в г/.из....... 0,010 0,018 0,030 0,051 0,081 ..... 0,59 1,07 1,78 3,04 5,00 Методы получения. Главная масса Н. получается из среднего и тяжелого масел-фракций каменноуго.льной смолы, кипящих в пределах 170-230° и 230-280°; первая из них предварительно подвергает- ся разгонке на карболовое (180-220°) и <-<нафталиновое масла. Последнее (с содержанием 45-50% Н.) разливается в кристаллизаторы, обычно плоские ящики- тарелки (как их называют в Донбассе) глубиной до 1 м, емкостью 1012 м^, в которых оно остается 2-4 суток (количество кристаллизаторов рекомендуется рассчитывать на 8- 10-суточную продукцию). За границей подобные тарелки устанавливают в несколько этажей в открытом с боков здании. На других з-дах, напр. в Англии, первую кристаллизацию Н. из горячего масла ведут в цилиндрич. резервуарах (обычно старых паровых котлах) емкостью 18-45 jn,снабженных змеевиком для глухого пара. После того как кристаллизация закончена, спускают оставшееся жидким масло и расплавляют Н. при помощи глухого пара. Расплавленный П. разливают в плоские кристаллизаторы, подобные упомянутым выше, для повторной кристаллизации. За границей в настоящее время применяют также искусствен-1юе охлаждение, причем кристаллизаторы снабжают мешалками, что значительно ускоряет процесс, и выделение П. происходит полнее. Дальнейшим шагом вперед является применение непрерывнодействующих кристаллизаторов. В Англии запатентован аппарат для кристаллизации П., состоящий из расположенных горизонтально один над другим цилиндрических сосудов, в ка-лодом из которых имеется концентрично расположенная труба со шнеком; внутренние трубы соединены последовательно между собой. По внутренним трубам течет нафталиновое масло, а между трубами-охлаледаю-щая лшдкость. Промышленного применения эти кристаллизаторы еще не нашли, хотя с успехом применяются для выделения парафина. По окончании кристаллизации Н. на тарелках дают маслу стечь через отверстие в дне тарелки, а кристаллич. массу Н. размалывают, подают в дезинтегратор и затем подвергают фугованию в центрифугах или прессованию в фильтрпрессах. После фугования в П. остается еще 2-4% масла. Варнес дает следующую производительность центрифуг в зависимости от размера: Диаметр барабана Производительность 750 лш............ 52-104 пг/ч 900 ............ 63-105 1050 ............ 76-152 После того как масло отфуговано, кристаллы промывают теплой водой (около 40°), способствующей, с одной стороны, расплавлению кристаллов /З-метилнафталина, плавящихся при 32°, а с другой-вытеснению масла, задерживающегося менсду кристал-.ыми Н. После фугования Н. подвергается прессованию в гидравлич. горячих прессах при давлении до 300 atm. В нек-рых случаях горячему прессованию подвергают сырой П. непосредственно после применения кристаллизаторов, но при этом Н. получается худшего качества, так как вследствие большего содержания масел сырой Н. имеет более низкую л ем фугованный; поэтому во избежание больших потерь Н. прессование приходится вести при более низких t°, что не благоприятствует удалению примесей. Если прессованию подвергается пафталин нефу- гованный, то рекомендуется, расплавив /з Н., смешать его с остальною частью и эту смесь прессовать. Прессование в настоящее время производится почти исключительно в прессах, подобных применяемым на маслобойных з-дах и имеющих для заполнения прессуемым П. два цилиндрас перфорирован-ньши стенками; в то время как один находится под давлением, другой выгружается и загружается вновь. Емкость цилиндра на прессах достигает 400 кг. Прессованный П., хотя и содержит относительно малое количество примесей и имеет Г . около 79°, но благодаря своему не вполне белому цвету с трудом находит сбыт, вследствие чего его необходимо подвергать дальнейшей очистке. Для этого нафталин дробят, расплавляют и (для удаления влаги) промывают 0,5-1% серной к-ты (60° Вё), затем 3-4% (от веса Н.) серной к-ты (66° Вё); после кислотной промывки следуют 2-3 промывки водой и наконец одна щелочная промывка раствором едкого натра (уд. вес ~ 1,17) для полной нейтрализации. Вся операция промывки продолжается 5-6 ч. Промытый Н. (предназначающийся для синтеза красителей и тому подобных целей) подвергают ректификации под вакуумом в кубе, снабженном мощной колонной. Холодильник наполняют горячей водой в 85-90° во избежание застывания Н. Скорость отгонки-1 500-2 500 л/ч. В результате получается ~ 90% чистого Н. Продукт, применяемый как средство от моли, не нуждается в такой тщательной ректификации и либо подвергается сублимированию .либо м. б. перегнан в простом кубе со шлемом; полученные кристаллы после измельчения могут быть спрессованы в шарики или кубики. Ниже приведены некоторые ориентировочные расходные коэфициенты, считая на1 m нафталина: Электроэнергия на центрифуги (для фугованного) .................... б kWh Электроэнергия на прессы (для прессованного) ...................... 60 Электроэнергия на дезинтегратор, воздух и мешалки при промывке (для промытого) . 21 и на 1 m ректификованного П.: Электроэнергия на дезинтегратор, воздух и вакуум при ректификации..........25 kWh Вода горячая для промывки на центрифугах 3 Вода горячая для холодильника при ректификации ..................... 9 л|3 Пар на горячее прессование.......... 0,20 m Пар на расплавление Н............ 0,1 Пар при ректификации Н........... 0,1 Применение. Н. поступает па рынок в виде сырого центрифугированного П., суб-.тпмированного Н. и прессованного в форме шариков, кубиков, плоских цилиндров и.ли чистого кристаллического нафталина. Эти сорта отличаются помимо внешнего вида гл. обр. чистотой и в зависимости от последней имеют различную t°nj.- В то время как сырой центрифугированный нродугст содер-лсит только 70-80% чистого П., содержание Н. в кристал.лич. продукте разнится от 100% лишь на несколько десятых %, а f° . лежит в пределах 79,5--79,6°. Сублимированный, а также и прессованный Н. содержит чистого П. 98-99%; t°j, их ок. 79°. За границей сырой центрифугированный Н. применяется в довольно значительных количествах в качестве горючего для автомоби- лей-как отдельно, так и растворенным в других видах жидкого топлива, напр. в бензоле, сшфте н т. п. Н. сублшдированный, или прессованный, применяется г.л. обр. в качестве средства от моли. Кристаллический чистый Н. используется в значительных количествах как исходный продукт для целого ряда промьпп.ленных органических синтезов, главным образом в производстве синтетических красите.чей, а такл-се взрывчатых веществ и некоторых фармацевтических препаратов. Другим потребителек Н. является промышленность искусственных смол, в ча-(зтности пзо.ляционных (г л и и т а .л е в ы е с м о .л ы, см. Глиптали) для э.лектротехнич. целей; при их получении исходным веществом служит фта.левый ангидрид, получаемый пз Н. За последнее время крупной областью применения Н. сдела.лось производство теуп-ралгта (см.) и декалина (см ), применяемых как весьма ценные растворители и в качестве горючего д.ля моторов. Кроме этого Ы. находит применение в военной технике как составная часть горючих дымовых смесей. Лит.: 1) Ан. П. 115906/17. -W а г п е s А., Coal Таг Distillation а. Working-up of Таг Products, 3 ed., L., 1923; Handb. d. Kokerei, hrsg. v. W. Glund, 2 Aufl., B. 2. Halle a/S., 1928; BunburyH. a. Davidson A., The Industrial Application of Coal Tar Products, London, 1925; см. также Ноксобензольное производство. Ф. Рыбкин. Производные Н. Встречаю1Щ1еся в природе немногие производные Н. не пмеют технил. значения. Из них юг л он (см. Красящие вещестеа естественные) находится в скорлупе грецкого ореха, с а и т о н и и--действующее нача.ло цитварного семени; гомологи Н.: метил- и диметилнафта.лип. а также а- и Д-наф-толы находятся в камонноуго.льном дегте. Наибо.льшее значение имеют синтетич. производные Н., получаемые введением в нафталиновое ядро различных групп (SO3H, NH2, NO ОН,галоидов и групп смешанны.: функций). Из них наибольшее значение имеют сульфопроизводные Н. Кроме главной области нрименения производных Н.-в синтезе красителей-они применяются п в других областям; так, ,б-су.льфокислоты--при приготовлении искусственного д>бителя Нерадоль ND (см. Дубильные .материалы); /З-нафтол применяется в медицине как ан-тисепгик. Эфиры ;8-нафтола с органическими к-тами применяются как кишечный антисептик: таковы: бензонафтол - эфир Д-нафто.ла и бензойной к-ты, б е т о л-эфир салици.ловой к-ты, л акт о.л-эфир молот-ной к-ты. Метиловый, этиловый и бутиловый эфиры /З-нафто.ла применяются в парфюмерии и известны иод названием wpo-лин (см.). В фотографии применяются производные -нафтола в качестве проявителей; таковы э и к о н о г е н (натриевая сол 1-амино-2-нафтол-0-су.льфокислота) и д и о-ген (натриевая соль 1-амино-2-нафтол-3,6-дисул ьфокислоты). Производные Н. в промышленности красящих веществ. Многие производные нафталина имеют исключительное значение в производстве азокрасителей. Особенно часто применяются сульфокис.лоты пафтиламинов, нафтолов, диоксинафталинов и аминонафтолов, количество к-рых весьма велико. В большин- стве случаев они являются продуктами обработки более простых производных Н., получаемых либо из нитронафта.линов либо из сульфокислот Н. Вследствие особенностей строения нафталинового ядра нри нитровании Н. имеет место введение нитрогруппы исключительно в а-положение. В силу этого большинство простейших замещенных производных Н. (в а-положении) получаются дальнейшей обработкой а-нитронафталипа или продукта его восстановления-а-нафтилами-на. С другой стороны, при сульфировании Н. более стойкой является его /З-сульфокис.лота (а-сульфокислота по.лучается при белее низких сульфогруппа в ней легко подвилша, переходя при более высокой t° в /З-пзомер). В виду этого большинство простейших производных Н., имеющих заместителей в 3-по-ложении, получаются дальнейшей обработкой )5-сульфокислоты И. В нафталиновом ряду весьма легко протекает реакция взаимного превращения гидроксильной группы в амидную и наоборот, вследствие чего .легко осуществляется получение а-нафтолов из а-нафтиламинов и )3-нафтиламинов из Д-наф-толов. Т. о. получение простейших производных Н. м. б. представ.лено следующ. cxcMoii: ,80зН NH.> Вышеприведенные реакции могут иметь место не только в простейших производных Н., но и в более сложных, где наряду с одной нитрогруппой или одной сульфогруп-пой имеются и другие заместители. Таким путем м. б. получены и более сложные производные аминов и фенолов нафталинового (как а, так и /3) ряда. Если такими заместителями являются сульфогруппы, то получаются сульфокислоты аминов и нафтолов. Сульфокислоты пафтиламинов и нафтолов м. б. также получены и непосредственным сульфированием готовых аминов и нафтолов. При нользовании обоими вышеприведенными методами, а такл:е реакцией взаимного перевода амидной группы в гидроксиль-пую ii наоборот, получается возможность приготовления значительного числа моно- и полисульфокислот обоих пафтиламинов и обоих нафтолов. Щелочное плавление некоторых из них приводит к сульфопроизвод-пым аминонафтолов и диоксинафтилинов. Наиболее валяные из су.льфокислот Н.: на-фтионовая кислота (1,4-нафтиламинсульфо-кислота), кислота Невиль-Винтера (1,4-па-фтолсульфокислота), к-та Шеффера (2,С-наф-толсульфокислота), R-кислота (2,3,6-нафтол-дисульфокис.лота), G-кислота (2, 6, 8-наф-толдису-льфокислота), Н-кислота (1, 8, 3, Ь-аминонафтолдисульфокислота), 1-кислота (2, 5, 7-аминонафтолсульфокис.лота), у-кислота (2,8,6-аминонафтолсу.льфокислота), хромс-троповая к-та (1,8,3, 6-диоксинафталин-дисульфокис.лота). Другие производные Н. применяются в значительных количествах как для синтеза красителей, так и в текстильной химии в ледяном крашении (см. Крашение). Таковы а-нафтиламип игл. обр. нафтоли (см.). Значение галоидонроизвод-ных Н. невелико. Об отдельных классах производных Н. и о методах их получения см. Промежуточные продукупы в синтезе красителей. Лит.: Борожцов Н. Н., Основы синтеза кра-сителей, М.,1925; его же, Ступени в синтезе красителей, Д., 1926,- F 1 е г Z-D avid Н.Е., Grundlegende Operationen d. Farbencbemie, 3 Aufl., В., 1924; R e-V e г d i n u. F u 1 d a, Naplitalinderivate, Basel, 1894; Tauber u. Norman, Die Derivate des Naphtalins, B , 1896, B. 29. И. Иоффе. НАФТЕНОВЫЕ КИСЛОТЫ, карбоксильн. производные нафтенов (см.); общая ф-ла их простейших представителей CnHa i-COOH. В более узком смысле под Н. к. понимают к-ты, встречающиеся в нефти или выделяемые из нее тем или иным способом; их называют тогда также нефтяными кис л от а м и. Подобно нафтенам Н. к. могут ирн-ладлелеать к различным циклич. рядам. Их рациональные названия должны указывать на природу циклич. ядра, а также на состав и пололееиие боковых групп. Так например, Н. к. со строением CH2 -СН9Ч сНз-сн -ель/ 1 2 )СН -солг д. б. названа 1,3-метплциклопентанкарбоно-вой кислотой. Вопрос о строении основного циклич. ядра Н. к. несмотря на многочисленные работы в этом направлении и поныне остается открытым. Молшо считать установленным лишь то, что простейшие естественные Н. к. в большинстве не принадлел1:ат к ряду циклогексана. Надо думать, что здесь преобладают пятичленные циклы, т.е. те кольчатые системы, которые занимают столь видное место в составе нафтеновой части естественных нефтей. П. к. представляют собой маслянистые жидкости с характерным запахом, особенно ненриятньш и прилипчивым у низших есте- ственных Н. к. Как типичные одноосновные к-ты, они легко образуют соли с одним эквивалентом основания и сложные эфиры с одной молекулой спирта. С трех- или пятихло-ристым фосфором Н. к. дают соответствующие хлорангидриды, превращающиеся при действии аммиака в кристал.лич. амиды; последними удобно пользоваться для характеристики Н. к., выделения их из неслол-ных смесей и очистки от примесей. По отношению к окислителям Н. к. очень устойчивы; окисление же при нагревапип приводит здесь лишь к продуктам глубокого распада. Н. к. совершенно не действуют только на алюминий и нек-рые специальные сорта стали и чугуна, но оказывают довольно значительное действие на другие металлы; наиболее сильно действуют Н. к. на свинец и цинк, менее всего-иа олово и железо. Простейший способ синтеза Н. к. заключается в действии уг.лекислоты на соответствующее магнийорганическое соединение, содерлсащее циклич. радикал. Так например, при действии СО, на магнийбромцикло-гексан, с последующим разложением проме-лгуточного комплексного соединения водой, получается циклогексанкарбоновая к-та: CgHiiMgBr-CeHii CO2H. Н. к. с шестичленными циклами м. б. получены также подобно нафтенам, путем гидрогенизации соответствующих ароматических соединений, т. е. бензойной кислоты (или ее эфиров) и ее гомслогов. Наконец Н. к. молено получать из природных нефтей, для чего смесь очищенных к-т подвергают этерифи-кации, и полученные слолшые эфиры, метиловые или этиловые, подвергают фракцио-нировке в вакууме, выделяя б. или м. узкие фракции. Так же, как в случае нафтенов, этим методом нельзя пользоваться для получения индивидуальных соединений; его применяют лишь Д.ЛЯ исследования химич. природы естественных нефтяных к-т. Содержание Н. к. в разных нефтях различно; о нем можно судить по кислотности нефтей (в % SO з). Так например, кислотностг> балахано-сабунчипской нефти (уд. в. 0,880- 0,882)ко.леб.лётся от 0,100 до 0,104% SO3, тогда как для различных сураханских нефтей кислотность иаб.людается лишь в пределах от 0,04 (красная сураханская) до 0,006% (белая сураханская Н|фгь). Как общее правило нафтеновые нефти заметно богаче кислотами, чем парафиновые. В дистиллатах одной и той же нефти Н. к. распределены также неравномерно. Наиболее богаты ими средние дисти.л.латы-соляровые и веретенные (около 2%), отчасти также и машинные (около 1,5%); керосиновые л^е и ци.линдро-вые дистил.латы содернсат Н. к. значительно меньше (0,4-0,5%). Получение Н. к. из нефти и ее дистил.латов производится обработкой последних едким натром с последующей обработкой щелочного раствора разбавленной серной к-той (см. Асидол). По.лучаемьк; таким образом И. к. содержат обыкновенно минеральные масла (до 25%); они употребляются преимуществеино при валянии шерсти, а также в качестве суррогата высших кислот жирного ряда при мыловарении. Их щелочные растворы, получаемые при очистке керосиновых дистиллатов ( щелочные отбросы ), утилизируются также для изготовления мылонафта; для этого их сначала, упаривают, а затем отсаливают поваренной солью и наконец продувают воздухом. Мы-.л о и а ф т хорошо мылится и характеризуется высокими дезинфицирующими свойствами; отрицательные качества мылонафта-жидкая консистенция и неприятный запах; для устранения его бы.ло предлолсено немало различнькс способов, к-рыми удается достичь б. или м. значительной дезодорации. Лит.: г у р в и ч Jl. Г., Научные основы переработки нефти, Москва, 1925; В и d о w s к i J., Die Naphtensauren, Berlin, 1922; N a p h. t a И M., Chemie, Technologie u. Analyse d. Naphtensauren, Stuttgart, 1927; A s С h a n O., Naphtenverbindungen, Ier-pene und Campherarten, 1929; Brooks В., Chemistry of the Non-Beuzenoid Hydrocarbons, New York, 1922. C. Наметкин. НАФТЕНЫ, термин, первоначально пред-лолсенный д.ля обозначения нефтяных углеводородов состава СцНги, об.ладающих характером предельных (Марковников и Огло-блин,Т881-83 гг.). Правильнее подразумевать под П. класс углеводородов непредельного состава, но с предельными свойствами, независимо от того, обнарул-сены эти уг.ле-водороды в нефти или нет. Простейшие П.. состав которых отвечает ф-ле CHan, характеризуются замкнутым (моиоциклическим) строением с 3, 4, 5, 6, 7 и более атомами углерода в цикле; их свойства напоминают свойства парафинов, вследствие чего Н. называются иногда циклопарафинами(см. Али-циклические соединения). Каждый простейший Н. стоит во главе особого ряда, объе-диняюш;его обширную группу производных данного цикла. Кроме Н. состава СпНа существуют также и Н. других рядов, например СпНг 4 ИТ. д.; они также обладают предельными свойствами, но по строению являются бициклическими или вообще полициклическими углеводородами. Хотя Н. составляют главную часть нек-рых нефтей (напр. бакинской), выделение их из этого природного продукта представляет гро-зтадные трудности и не может служить источником получения чистых Н. (см. Нефть). Для получения отдельных представителей II. применяются следующие синтетич. методы. 1) Действие металлич. натрия на некоторые дибромиды или цинковой пыли на их спиртовый раствор; этим путем получаются напр. циклопропан (Фрейнд, 1882 г.) и его гомологи: СНг BrCH2-CH..GH2Br+2Na= +2NaBr. НгС СНз дибромпропан циклопропан 2) Восстановление нек-рых галоидонроиз-водных, получаемых в свою очередь из соответствующих спиртов или кетонов. Послед-юте могут быть получены проще всего сухой перегонкой двуосновных к-т жирного ряда или их солей, напр.: HiC сн. адипиновая к-та циклопентанон Этим способом был приготовлен впервые синтетич. П., находящийся в кавказской нефти, 1, 3-диметилциклогексан (Зелинский, 1895 г.), а также позднее обнаруженные в нефти циклопентан (Вислиценус, 1893 г.), ци1слогексан (А. фон-Байер, 1893 г.) и многие другие П. 3) Наконец П. с шестичлеп-ными циклами и их производные удобно получаются гидрогенизацией соответствую-иц1х ароматич. соединений (см. Гидрирование). Этим способом широко пользуются в настоящее время для технич. превращения ароматич. углеводородов и их производных в соответствующие производные нафтенового ряда; так например, из фенола CeHgOH получают циклогексанол СеНцОН; из нафталина CioHg-декалин СюН^д и тетралин CioHia, и т. д. По своим химич. свойствам Н. напоминают более всего парафины; подобно последним они совершенно неспособны к реакциям присоединения. Исключение составляют лишь Н. низших рядов, напр. циклопропана; так, сам циклопропан, присоединяя иодистоводородную к-ту, дает йодистый пропил и т. п. Подобно парафинам Н. при действии хлора дают хлорозамещенные продукты, со слабой же азотной кислотой при нагревании образуют нитросоединения предельного характера; кроме того в этом последнем случае получаются и продукты окисления Н.-соответствующие двуосновные к-ты; так, из циклопентана получается СНг-СНз-СООН I =Но0+С0.,+ СНз-СНа-СООН глутаровая кислота, из циклогексана-ади-нинозая ИТ. п.: НгС СН2 НаС СНз циклогексан СНз-СНг^СООН СНа-СНз'СООН адипиновая к-та Д.1я шестичленных П., напр. циклогексана и его гомологов, характерна также способность перехода в ароматич. углеводороды в. присутствии тех же катализаторов, к-рые содействуют гидрогенизации бензола и его гомологов, но при бо.лее высокой температуре (ок. 350°). Лит.: Г у р в и ч Л. Г., Научные основы переработки нефти, Москва, 1925; 3 а п к и н д Ю. С, о составе нефтей, Нсфт. и сланц. хозяйство , М., 1922; Наметкин С. С, Очерк развития взглядов на углеводороды кавказской нефти, там же, 1921; А S с h а п о., Chemie d. alizyklischen Verbindungen, Braunschweig, 1905; Aschan 0., Naphtenverbin-dungen, Terpene und Campherarten, inkl. Pinusharz-saure sowie KOrper d* Kautschukgruppe, Berlin, 1929; Brooks В., Chemistry ol the Non-Benzcnoid Hydrocarbons, New York, 1922. C. Наметки . НАФТИОНОВАЯ КИСЛОТА, 1, 4-нафт11л-аминсульфокислота, применяется в производстве красителей. См. Промежуточные продукты синтеза красителей. НАФТОЛ Ы, оксипроизводные нафталина, э.лементарного состава СюН^О, широко применяемые в качестве промежуточных продуктов синтеза красителей (см.) и в текстильной химии для ледяного крашения (см.). Существуют два изомера Н. 1) а-Нафтол, получаемый сплавлением со щелочами а-сульфокислоты нафталина или же гидроксилированием а-наф-тиламина; белый кристаллич. продукт с 1°пл. 96 , t\ , 278-280°, уд. в. 1,224, трудно растворимый в воде, легко - в органич. растворителях. Применяется в производстве красителей п для превращения в более сложные производные нафталина (см.). 2) /3-Н а ф т о л является одним из наиболее важных промежуточных продуктов в синтезе красителей, получается при сплавлении со щелочами Д-сульфосоли нафталина и очищается перегонкой с перегретым водяным паром или в вакууме; белый кристаллич. продукт с t\,. 122°, 285 -286°, уд. в. 1,217; трудно растворим в воде, легко-в органич. растворителях. Применяется для производства азокрасителей и изготовления более сложи, производных нафталина, как нитрозо--Н. и сульфокислоты /3-Н.; особенно велико применение /З-Н. в ледяном крашении. 3) Н а ф т о л ы AS. Под этим названием-фирмой Грисгейм-Электрон были вынущены. производные 2,3-оксинафтойной к-ты -он соон которые более применимы в ледяном крашении, чем Д-Н., так как дают более яркие и прочные оттенки и облегчают самый процесс ледяного крашения; нафтолы AS обладают субстантивными свойствами и в силу этого адсорбируются волокном. В виду этого хл.-бумажные ткани, обработанные раствором нафтола AS, могут без предварительной просушки быть пущены на обработку раство- 1 ... 15 16 17 18 19 20 21 ... 48 |
|
© 2007 SALROS.RU
ПромСтройМат |