 |
 |
 |
 |
1 ... 18 19 20 21 22 23 24 ... 49 Кениг в своих изысканиях исходит именно из таких соединений, - например солей оснований общей ф-лы \N-(CH), -i:-N/ где R и Ri-любые радикалы, а X-какой-либо анион, напр. С1. При п=3 имеем следующее соединение (изображая его строение классической структурной формулой) СН: - СП-СП-СП-CH-N -лт/ \ Подобного рода соли образуются присоединением например галоидного алкила RjX к имидооснованиям. Так как подобные соли проводят электрический ток, то, согласно теории Вернера, анион X должен лежать отдельно от Ri, во второй координационной сфере ~>N-CH-СН-СН:=СН-СН-n( На обоих концах цепи получаются так. обр. совершен-/R но идентичные группы - N , т. е. ауксохромы. По- следние же способны обнаруживать, сверх нормальной валентности их центрального атома, одинаковые количества положительной и отрицательной дополнительной валентности, т. е. имеют характер диполей. Аниоп X, обладающий отрицательным зарядом, д. б. , связан с остальной частью молекулы (комплексным катионом) ослабленной связью, на которую затрачивается неполная его валентность R . - /R >N-СИ-СН-СН-СН-СН-N( R,/ ---- \r, Предположим (произвольно), что X связан неполной связью с правым (в ф-ле) атомом N. Последний, переходя из трехвалентного состояния в пятивалентное, обнаруживает, сверх нормального, одинаковые количества положительного и отрицательного сродства (равные по величине заряды н- и -). Положительный побочный заряд нейтрализуется отрицательным зарядом аниона, но не полностью, т. к. анион связан лабильно. Остаток этого положительного заряда связывает часть остающегося у азота отрицательного заряда, остальная же часть последнего затрачивается на образование второй связи между N и метиновой группой; эта вторая связь является тоже ослабленной (неполно!!). Со стороны первой метиновой группы на образование этой связи расходуется также неполный положительный заряд, часть которого, оставаясь неиспользованной, оттягивает на себя часть отрицательного заряда второй метиновой группы, и т. д Таким образом в конце-концов индуцируется частичный положительный заряд у пятой метиновой группы, берущий на себя часть побочного отрицательного заряда атома N второго ауксохрома (левого в формуле). У азота этого ауксохрома также останется следовательно нек-рая свободная часть положительного заряда, которая может быть затрачена на нейтрализацию остаточного отрицательного заряда аниона. Иными словами, получается замкнутая цепь подвижных гете-рополярных связей, изображаемая следующей ф-лой, в которой ослабленные связи представлены волнистыми линиями, а остаточные частичные заряды соответственных атомов знаками -ь и - Rv--!- - + - + - ,R )N;CH--:::CH:,:CH-СН-г-СН-N( Ri + 5 + Ri Внутри этой цепи, вследствие лабильности частичных связей, происходит постоянное смещение валентных электронов с одной орбиты на другую, вызывающее эффект светопоглощения. Чем длиннее цепь, т. е. чем больптее число отдельных силовых полей этих электронов частично перекрывает друг друга, тем большее влияние оказывают колебания одних электронов на другие, взаимно замедляя друга друга. Поэтому для перемещения электронов на их крайние внешние орбиты требуются такие кванты энергии, которые м. б. получены лишь от световых лучей с достаточно большой длиной волны. Соответственно, с удлинением цепи конъюгированныхметиновых групп, абсорбция света перемещается все больше в область лучей красной части спектра. Сопряжение с анионом двух крайних ауксохромов, представленное на приведенной выше ф-ле, соответствует максимуму поглощения, лежащему всего ближе к красному концу спектра; однако можно допустить, что частичные отрицательные заряды аниона м. б. нейтрализованы частичными положительными зарядами всякой другой пары групп, напр. зарядами одного из ауксохромов и метиновой группы 1-й, 3-й или 5-й. В последнем случае образуются две (или более) замкнутые цепи, служащие причиной абсорбции света с меньшими длинами волн, например: R ч - + N;X Н -С П:с С Н-С Н:::сС H=;N Возможность замыкания более коротких цепей дает начало новым абсорбционным полосам в спектре. Поэтому существуют тела с 2, 3 и более максимумами поглощения света. Аналогично трактуются Кенигом соли с катионами во внешней сфере; напр. соединение О-СН-СНСН-СН=СН-ONa изображается так + - + - + 0~СНз::СН-СН-СН.-СН:=:;0 При разнозначных крайних ауксохромах может происходить внутреннее замыкание и без помощи аниона или катиона, например -f - + О,-С Н-С Н::СН:СН -Г-Т1-СН- - - ,R Перенося эти воззрения на более сложные цветные соединения, Кениг приходит напр. к следующей ф-пе для основных трифенилметановых красителей Н Н II ПН С-С + С-с - +\ I И Н Н И > Теория Кепига, наиболее сог.ласованная с теорией строения атома и с современными воззрениями на природу светопоглощения, хорошо объясняет многие явления в области цветности органич. соединений, но не получила еще полного развития в приложении ко всем цветным телам. Классификация красителей. Так как большинство красителей, при условии допуше-ния таутомерии их, можно считать хиноида-ми, то представляется весьма удобным классифицировать синтетич. К. в. по типам за-ключаюшихся в них хиноидных колец. Эта, хотя и не вполне точная, классификация представляет большие удобства для запоминания и для обобшений в области синтеза; она м. б. легко перестроена как на более старую классификацию по хромофорам, так и на классификации по типам комплексов, по осцилляциоиным типам и на кенигов-скую (см. выше). Все синтетич. К. в. можно разделить на следующие классы. I. Хинонные красители, характеризуемые присутствием в их молекуле п- или о-хинонного кольца (или половины последнего) 1=0 \с=с{ ли I J-0 или \с О 1) Индиго и индигоиды. 2) Нафтохинонные красители. 3) Антрахинонные красители. II. X и н о н о к с и м н ы е, характеризуемые наличием п- или о-хиноноксимной группировки О^О-ОН или 1) Нитрозокрасители (хиноноксимы) .2) Ни-трокрасители. III. Хинонгидразонные, характеризуемые присутствием группировок и N-NHR или - N NHR .=N-NHR или -r-NRi J-N NHR 1) Гидразонпиразолоновые красители. 2) Азокрасители. 3) Стильбенов. красители. IV. Хинонимидные и хинон-диимидные, характеризуемые присутствием группировок 0=<(-NR или (111 или RiN=<=NR -NRi =NR 1) Инд амины и индофенолы. 2) Азины и азонии, черный анилин, оксазины и тиази-ны. 3) Сернистые красители. V. Метиленхинонные имети-ленхинонимидные, характеризуемые присутствием групп или 1=0 R или С=:< N=NR2 или Ri/ -/ J NRRi 1) Трифенилметановые. 2) Акридиновые. 3) Ксантеновые. 4) Оксикетонные и кетон-имидные (дифенилметанов.) красители. 5) Хи-нолиновые красители. Класс I. Хинонные красители. Fpynnal. ИндигоидныеК. В. (красители полухинонного типа). Они получили свое название от старейшего представителя этой группы-синего индиго (см.) .NH4 ,NHv \ / с=с со/ СО и заключают всю свойственную его молекуле полухинонную группировку атомов I I ос с=о \ / с=с Подобно тому как w-хинон по своим химическим свойствам м. б. отнесен одинаково как к v-дикетонам, так и к перекисям и принимается б. ч. за соединение таутомерное, существующее в обеих этих формах: П o-f ~)-о так же и индигоиды м. б. представлены в двух таутомерных формах II I I . I о о о--о I. II. Существованием перекисной формы (II) естественнее всего объясняется свойство всех индигоидов легко восстановляться в лейко-соединения (см.), имеющие след. строение с-с и Подобно гидрохинону, являющемуся лейко-соединением хинона, и щелочнью растворы лейкосоединений индигоидных К. в. легко окисляются в красители, нерастворимые в воде. На этом основано и крашение ими различных волокон (см. Крашение). Что касается цветности этих красителей, то между ними встречаются вещества всех цветов видимого спектра, но лишь немногие из них дают окраски ходовых оттенков. Цветность ивдигоидных красителей, по теории Витта, зависит от присутствия в них трех хромофорных групп: двух групп =С-О и одной -CR=CR-, соединенных с двумя ароматическими ядрами, и ауксохромных групп NH-, -S-, -О-, внедренных между хромофором и ароматич. ядром. Теория хиноидного строения приписывает цветность индигоидов наличию полухи-нонной группировки (включающей все три хромофора Витта) и связанных с нею ауксохромных групп. По Кенигу, можно было бы представить например индиго в стедую-щем виде  что в упрощенном виде выражается и тауто-мерной ф-лой индигоидов, приведенной выше. Рациональная классификация индигоидов приведена в ст. Индигоидные красящие вещества. По строению и методам получения индигоидные К. в. могут бьггь разделены на симметричные и несимметричные. Первые обьшно получаются окислением двух молекул одного и того же вещества, вторые же-конденсацией двух различных компонентов. К первьпл следует отнести 2, 2-бис-индолиндиго, 2, 2-бис-нафт-индолиндиго, 2, 2-бис-антриндолиндиго, а также соответствующие тионафтеновые и другие производные. Второй отдел охватывает несимметричные индигоиды, как 2, 3-бис-индолиндиго (индирубин), 2-тионафтен-3 -индолиндиго(тиоиндиго алый R) и другие. Среди индигоидных красящих веществ доминирующее значение имеют красители, содержащие по два пятичленных цикла; но существуют и такие, которые имеют только один пятичленный цикл либо вовсе не имеют такового. При получении как симметричных, так и несимметричных индигоидов необходимо заранее синтезировать про-менхуточные продукты, содержащие замкнутые, характерные для этих красителей циклы: индоксил, изатин, изатинанилид, 3-окситионафтен и т. н. В промежуточных циклических соединениях, служащих для получения индигоидов, является характер-ньпл наличие кетоэнольной таутомерии. Це-льп! ряд соединений, способных к кетоэнольной таутомерии, м. б. применим в качестве промежуточных продуктов для синтеза индигоидов. Наиболее важными исходными веществами являются а-нафтол (I), оксиантра-цен (II), оксиантрахинон (III) и ряд хинонов он о он о 00-СО 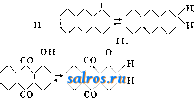 III. о получении индоксила, изатинанилида и изатина см. Индиго, тиоиндоксила-см. Индигоидные красящие вещества 3-окситионафтен, важный полупродукт синтеза индигоидов, получают по способу Фридленде-ра, исходя из антраниловой кислоты, или по способу Герца, исходя из анилина и дву-хлористой серы, причем происходит как хлорирование анилина, так и внедрение в бензольное ядро серы. Полученный продукт при восстановлении переходит в производное о-аминотиофенола, к-рое с хлоруксус-ной к-той дает соответствующее глициновое производное, после чего, по реакции Занд-мейера, через нитрил получается карбоно-вая к-та. Последняя при действии водоотни-мающих средств переходит в производное окситионафтенкарбоновой кислоты. Так, для случая о-толуидина получается 4-метил-6 - хлор - 3 - окситионафтенкарбоновая к-та, важный продукт для синтеза гидрона розового, по схеме СНэ -NHa + S2CI2 С1У S-Cl СНз СНз -NHa [Л-Нг ск - Cl/ СНз СНз 0-CN /N-COOH -S-CHa-COOH /l-SCHa-COOH r g))G.cooH СНз CHs I :-С0\ /СО- g/0-CS- Ci/\ ~- V NCI гидрон розовый Существует много аналогичных способов синтеза производных 3-окситионафтена [2]. Интересен также способ получения изомер- ного продукта из того же о-толуидина по следующей схеме СНз СНз СНз -NHj СНз -NH2 С1/ (с ксантогенатом) СН. I-S-CS-OCjHs Cl/ СНз -s-СНа-соон -С(ОН). СН- - -С0\ у СНз СНз гелиндоновый красный ЗВ Для получения индигоидов кроме вьше-перечисленных продуктов могут служить и их нафталиновые и антраценовые аналоги, получаемые общими методами. Для нафталиновых и антраценовых производных возможны по три изомера, нанрим. для нафт-индоксила СОН-СН NH-сн а также и пери-производное НОС NH -СОН дающие различные изомеры нафтиндиго. В последние годы изучение подобных нафталин-и антрацениндигоидных К. в. приобретает все большее значение. Из других продуктов для синтеза индигоидов применяются оксипроизводные-нафтолы, нафтохино-ны, аценафтенхиноны, антранолы, оксиан-трацены и др.; сочетая их с различными производными индола и тионафтена, можно получать различные индигоиды как симметричные (окислением двух одинаковых молекул), так и несимметричные (при сочетании двух различных молекул); в последнем случае один из компонентов представляет собою обьгано а-дикетон или о-хинон (вернее, его производное), второй же-какое-либо циклическое оксипроизводное, способное к кетоэнольной таутомерии. Так, краситель типа о м. б. получен либо конденсацией изатинанилида с нафтолом, реагирующим в кетоформе о н QInh>=c +h>()Q-> -> CeHjNHa + краситель либо путем конденсации индоксила (реагирующего в кетоформе) с 1, 2-нафтохиноном о -С0\ 0= -NH/ + Н 2 о-Ь краситель 1. Симметричные индигоиды. Важнейший представитель-индиго, 2, 2-бис-индолиндиго-см. Индиго. Т и о и н д иго красный, 2, 2-бис-тионафтенинди-го, получается при окислении двух молеку.т 3-окситионафтена или непосредственно, по Мюнку, замыканием колец в ацетиленди-тиофенол-о-карбоновой кислоте, по схеме + С1СН:СН-С1 i-cooiT liooc- -s\cc/s Индигокармин, 5,5-дисульфокис-лота индиго, получается при действии концентрированной H2SO4 на индиго или на фе-нилглицин; применяется мало, как кислотный краситель и для титрования при анализе гидросульфита (см.). Индиго 2R, 5, 5 -диброминдиго, получается при умеренном бро-мировании индиго или синтезом из бром-индоксила; обладает несколько более красным оттенком, чем обыкновенный индиго. Индиго 4В, 5, 7,57-тетраброминдиго, получается при бромировании индиго в ки-пяшем нитробензоле; более чистый по оттенку и более прочный краситель, чем индиго. Индиго 6В, 4, 5, 7, 4, 5, 7-гексабром-индиго, получается при действии избытка брома на индиго под давлением; применяется иногда в печатании, дает зеленовато-синие оттенки. Яркий индиго различных марок-хлор- и хлорбромпроизводные индиго, получаемые при хлорировании де-гидроиндиго Кальба (см. Индиго). Инд иг о Т, 7, 7-диметилиндиго, получается аналогично индиго, синтезом из о-толуидина или из о-нитрометилбензальдегида; окрашивает ткани в более зеленый цвет, чем индиго. Циба красный разных марок -- гало-идо производные тиоиндиго, получаемые при галоидировании тиоиндиго. Гидрон розовы й-см. выше. Тиоиндиго оранжевый, 6, б'-диэтокситиоиндиго, получается при окислении 6-этокси-З-окситио-нафтена. Кроме того в продаже имеется ряд различных галоид о-, окси-, амино-, этокси- и метокси-производных раз'личных симметричных индигоидов, получаемых обьганьши путями. Ряд производных индиго и тиоиндиго, содержащих вместо бензольных ядер нафталиновые и антраценовые, находится в настоящее время в стадии изучения; из но.лу-чивших практич. применение представителей этого ряда необходимо отметить тиоиндиго зеленый G, дибром-бис-нафтиндолиндиго строения вг-/\ /\-В1 \/-NH/ \хм1- ОН получается при бромировании нафти-затинаи обработкой бромопродукта по бай-еровскому способу превращения изатина в индиго. 2. Несимметричные индигоиды. Простейший из них - индирубин, 2, 3- бис-индолиндиго, сопутствует индиго- тину в естественном индиго и м. б. получен синтетически при конденсации изатина с индоксилом. Практич. применение имеет его 5, 7, 5, 7-тетрабромпроизводное-ц и б а-гелиотроп В. Аналогичный индиру-бину тиоиндиго алыйК, 3-индол-2-тионафтениндиго, получается при конденсации изатина с окситионафтеном. Если вместо изатина взять его 2-анилид, то получается циба серый, 2-индол-2-тионафтен-индиго; практическ. применение имеет только его тетрабромпроизводное циба фиолетовый В. Из непятичленных циклич. соединений находят применение следующие. Ализар ин-индиго 3R-трибромпроизводное 2-ин-дол-2-нафтолиндиго, получаемое при конденсации дибромизатинанилида с бром-а-на-фтолом; мало применяется (в печатании), прочен к хлору и мылу. Ализарин-индиго G - дибромпроизводное 2 - ин-дол-2 -антрацениндиго, получаемое при конденсации дибромизатинанилида с а-антро-лом. Ализарининдиго 2G, 2-ин-дол-2-оксантролиндиго, получается при конденсации изатинанилида с оксиантрано-лом. Циба алый 2G, 2 - тионафтен-2-аценафтениндиго, получается при конденсации окситионафтена с аценафтенхино-ном. Ряд красителей несимметричных, содержащих в различных сочетаниях нафтин-долы, антриндолы и их сернистые аналоги, находится в стадии исследования. Индигоидные красители нерастворимы в воде и поступают в продаи-су в виде порошков или водных паст, содерл-сащих чаще всего ~20% сухого красителя. Все они принадлежат к так наз. кубовым красителя.ч (см.), окрашивание которыми основано на восстановлении красителя в растворимые в щелочах лейкосоединения, пропитывании волокнистых материалов растворами этих лейкосоединений и обратном окислении их в нерастворимые красители на волокне кислородом воздуха. Лейкосоединения индигоидов 6. ч. желтого или оранжевого цвета, т. е. окрашены значительно выше самих красителей, что объясняется разрушением в них хромофорной группировки -ос-Сгс-со- I i Окраски, получаемые при помощи индигоидных красителей, почти все отличаются большой прочностью как к свету, так и к мылу и другим реагентам (к-там, щелочам и т. д.). Лишь к трению нек-рые окраски (в том числе и самое индиго) не вполне прочны, что объясняют механ. характером связи их с волокном. Наиболее распространенным красителем этой группы является самое индиго. Другие индигоиды применяются в значительно меньшем масштабе, гл. обр. вследствие своей высокой цены и сравнительно высокой стоимости крашения ими, требующего применения гидросульфита. Группа II. Нафтохинонные красители. Практически годные красители, заключающие бензохинонное кольцо, неизвестны. С технически важными К. в. хинон-ного типа мы встречаемся лишь в нафталиновом ряду. Первьш (и самым важным) пред- ставителем этой группы является н а ф та 3 а р и н, 1, 4-ДИОКСИ-5, 8-нафтохинон получаемый нагреванием 1, 5- или 1, 8-ди-нитронафталина с крепкой серной кислотой и S2O3 (раствором серы в серной кислоте), причем происходит сначала восстановление групп-NO2 в-NH-OH, затем перегруппировка образовавшегося дигидроксиламин-нафталина в диаминодиоксинафталин, окисление последнего в динафтохинондиимид, омыление этого диимида в нафтодихинон и наконец восстановление нафтодихинона в ди оксинафто хино н Цветность антрахинонных красителей обусловливается, согласно хромофорной теории , присутствием двух хинонных карбони-лови различивши ауксохромными группами: -ОН,-NH-,-SR и т. д. Но среди кубовых антрахинонных красителей встречаются и такие, которые совсем не имеют виттовских ауксохромов, напр. пирантрон, виолантрон и др. Т. о. присутствие ауксохромных групп не является обязательным для красителей, если не принимать за ауксохромы метиновые группы, входяшие в состав ароматич. ядер. Кубовые красители, к к-рым принадлежат пирантрон, виолантрон и др., нерастворимы в воде и в строгом смысле слова К. в. не являются, так как они либо совсем не усваиваются волокном, либо не дают того цвета и интенсивности, какие получаются при обычном кубовом крашении; настоящими N0.; NHOH но NH2 I I 1 о NH NO3 NHOH H2N он O2N NOa HOHN NHOH HgN NHg HO OH в виду нерастворимости нафтазарина в воде его обработкой бисульфитом натрия переводят, для применения в крашении, в бисуль-фитное производное но OSOaNa /\ он NaOgSO он которое при крашении разрушается с регенерацией красителя. Нафтазарин принадлежит к протравным красителям и дает по хромовой протраве глубокосиние, почти черные тона, почему он и называется часто ализариновым черным S или SW . Окраски им отличаются большой прочностью. Глубокий синий цвет окрасок по протраве объясняется образованием внутренней комплексной соли с хромом. Вообще же цветность нафтазарина относят за счет СО-групп (хромофоров) хинониого ядра и гидроксильных ауксохромов (или, по хиноидной теории, за счет всего хинонного ядра и гидроксилов). Кроме нафтазарина известны: нафтоп ур-пурин, 1,2, 4-триокси-5, 8-нафтохинон, получаемый окислением нафтазарина, и некоторые производные нафтазарина, замещенные в хинонном ядре остатками фенола или анилина (ализариновый темнозеленый W, ализариновый черный SRA). Группа III. Антрахинонные К. в. Эти красители представляют собою производные антрахинона (см.) о о !1 I HN о HN NH О О о ОН О О красителями, непосредственно усваиваемыми волокном, служат здесь лейкосоединения, заключающие обычно группу-ОН. Вантра-хинонном ряду эти лейкосоединения по цветности часто не только не уступают самим красителям (индантрен),но иногда являются даже глубже окрашенными (желтый флавант-рен, имеющий синее лейкосоединение,и другие). Сточки зрения теории хиноидного строения носителем цветности этих К.в. является центральное хинонное кольцо антрахинона. Интересно отметить явления таутомерии среди антрахинонных красителей. Найдено например, что ализарин при попытке этери-фицировать его в щелочном растворе галоидными алкилами дает не ожидаемый эфир (I), а этерифицированное в мезо-положение производное (II) о л„ о \/>-0СНз 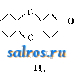 с правьпк! кольцом, построенным пара-хи-ноидно (В. Неркин мл.), из чего можно заключить, что и щелочные соли ализарина могут существовать в таутомерией 9г-хино-идной форме. С точки зрения осцилляцион-ной гипотезы цветности такая возможность таутомеризации, обусловленная присутствием ауксохромов, давая начало новьиг осцилляциоиным формам, служит причиной значительного углубления цвета по сравнению с самим антрахиноном. По теории Кенига, соли ализарина могут быть изображены следующим образом:  Синтез ализарина по Гребе и Либермапу (из антрацена, через;3-антрахинопсульфокислоту)до настоящего времени является единственным широко применяемым техническим методом получения синтетич. ализарина. В 1871 году Ирюдом получил конденсацией амино-ализарина с глицерином весьма ценный краситель- ализариновый синий, положив тем самым начало синтезу ряда сложных циклических производных аптрахинона. В 1887 году Бонн и одновременно с ним Шмидт заметили способность ализарина и его производных превращаться при действии окислителей в присутствии катализаторов в различные полиоксипроизводные (см. Бонна-Шмидта реакция), что позволило обогатить группу антрахинонных К. в. весьма ценными протравными красителями. М. А. Ильинский впервые провел сульфирование аптрахинона в присутствии солей ртути, получив при этом а-сульфопроизвод-вые, что позволило получать в большом масштабе целый ряд ценных а-производных аптрахинона, В начале 20 века Бонн получил и первый антрахинонный кубовый краситель, индантрон, и вслед за ним фла-вантрон, исключительная ценность которых направила исследовательскую мысль по новому руслу кубовых антрахинонных красителей. В 1905 году Излером был получен антрафлавон и Шоллем-пирантрон. Год спустя Шолль получил виолаптрон, положив этим начало группе ценных бензантроновых красителей. В это же время Ульман ввел в употребление реакцию конденсации аминов с галоидопроизводными в присутствии меди, давшую возможность синтезировать ряд ценных красителей ряда антримидов. В 1909 году Дейнет получил бензоильные производные аминоантрахино-нов, оказавшиеся ценными альголевыми (индантрено-выми) красителями. За сравнительно короткое время аитрахинонные К. в. заняли одно из важнейших мест среди синтетич. красителей и значение их возрастает из года в год. По технич. применению аитрахинонные К. в. делятся на два класса: кислотные (т.о. протравные) и кубовые. Первые из них м.б. разбиты на два больших отдела: а) оксиан-трахинонные красители, к-рые могут кроме ОН-групп содержать и замещенные NH2-, SH-группы и т. п., и б) красители, содержащие сульфогруппы как в антрахинонном ядре, так ивне его.Оксиантрахинонные красители являются преимущественно протравными и применяются для окраски предварительно протравленных металлич. окислами волокон; сульфоантрахинонные же красители благодаря наличию в них ЗОзН-групп способны непосредственно окрашивать волокно животного происхождения; при этом они зачастую могут давать при последующей обработке солями хромовой кислоты прочные яркие лаки и применяться как хромировочные красители. Кубовые аитрахинонные красители по их химич. строению м. б. разбиты на два отдела. К первому относятся те красители, в к-рых наиболее слоясным циклом является цикл антрацена и к-рые получаются конденсацией нескольких антрахинонных производных между собой или с более простыми соединениями, конденсацией, не сопровождающейся образованием новых колец; наиболее простые красители этого класса-альголевые красители-представляют собою ацильные, преимущественно бензоильные, производные аминоантрахинонов; более сложные-антр- Т. Э. т. XI. имиды-содержат по крайней мере 2 антрахинонных остатка, соединенных в различных положениях имидными группами. Второй отдел кубовых антрахинонных красителей содержит различные многоядерные циклы как карбоциклического, так и гетероциклического типов, что мож;ет служить основой для их классификации. Общая классификация антрахинонных К. в. в силу из-лолеенного выше является следующей. 1. Кислотные красители. А. Оксиантрахинонные красители. Б. Сульфированные аитрахинонные красители: 1) содержащие сульфогруппу в антрахинонном ядре, 2) содержащие сульфогруппу вне антрахинонного ядра. 2. Кубовые красители. А. Собственно аитрахинонные красители: 1) ацильные производные аминоантрахинонов, 2) антримидные красители. Б. Многоядерные красители: 1) содержащие гетероциклич. ядра; 2) содержащие кар-боциклич. ядра: пиреновые производные и периленовые производные. 1 А. Кислотные оксиантрахинонные красители, содержащие ОН-группы, являются протравными красителями в силу наличия в них способной к лакообразованию группировки (правило Либермана и Костанец-кого), именно двух ауксохромных групп в о-положениях друг к другу и к хромофорному карбонилу. Это правило не является законом,обусловливающимпротравные свойства красителей, но в большинстве случаев лишь при выполнении его по.лучаются технически применимые протравные К. в. Некоторые полиоксиантрахиноны, не обладающие подобным расположением оксигрупп, не представляют собою красителей, но являются ценными промежуточными продуктами для синтеза более сложных антрахинонных красителей. Ниже приведена таблица наиболее важных полиоксиантрахинонов с указанием цвета лаков для тех из них, которые применяются в качестве красителей. Положение оксигрупп указано номерами углеродных атомов, ири которых они находятся, причем молекула аптрахинона перенумерована обычньпй образом 8 1 7/\/°\/\2 i I I L 10 * Как видно из таблицы, увеличение числа ОИ-групп, за исключением производных галловой к-ты (антрагаллол и руфигаллол), вызывает углубление цвета лаков красителей. Все полиоксиантрахиноны способны давать с к-тами эфиры, из к-рых борнокислые эфиры обладают характерным для каждого по-лиоксиантрахинона цветом и спектром поглощения, чем и пользуются при контроле производства, чаще всего при проведении Бонна-Шмидта реакции (см.), для суждения о ходе реакции. Общие методы получения полиоксиантрахинонов м. б. разбиты следующим образом. 1) Щелочное плавление сульфокислот аптрахинона или омыление его галоидопро-изводных. Щелочное плавление сульфокислот часто сопровождается и окислительным и Полиоксиантрахиноны. Рациональное наименование Эмпирическое наименование (торг. марка) Цвет лака 1, 2-диоксиантрахинон 1, 4- 1, 5- 1, 8- 1, 2, 3-триоксиантрахинон 1, 2, 4- 1, 2, б- 1, 2, 6- 1, 2, 7- 1, 2, 5, 8-тетраоксиантрахинон 1, 3, Ь, 7- 1, 2, 3, 5, 8-пентаоксиантрахинои 1, 2, 3, 5, 6, 7-гексаоксиантрахинон 1, 2, 4, 5, 6, 8- 1, 2, 4, 5, 7, 8- Ализарин Хинизарин Антраруфин Хризазин Антрагаплол Пурпурин Яркий ализарин-бордо R Флавопурпурин Антрапурпурин Хинализарин Антрахризон Ализарин-цианин 2R Руфигаллол Ализарин-цианин WRR Ализарин-цианин R Оливково-корич-невый Желто-коричн. Красно-коричн. Сине-фиолетов. Сине-фиолетов. Фиолетовый Коричневый Синий Синий Фиолетовый Красный Желтый Алый Сине-красный Желтовато-красный Желтовато-красный Синеватый бордо Красновато-фиолетовый Коричневато-желтый Фиолетовый Фиолетовый образованием гидроксильн. группы в о-поло-жении к вступающей в реакцию сульфогруп-пе; в тех случаях когда необходимо избежать этого, плавление производят не с едкими щелочами, а с гидратами окисей щелочноземельных металлов, чаще всего с известью. Примером может служить получение ализарина (см.) из солей /3-антрахинонсульфо-кислоты при сплавлении ее с щелочами или с известью. 2) Конденсация производных фталевого ангидрида с оксипроизводными бензола и замыкание антрахино НПО го цикла в получившемся при этом оксипроизводном бензоил-бензойной к-ты. Этот способ наиболее часто применяется при получении оксиантрахино-нов с ОН-группами лишь при одном бензольном ядре антрахинонного цикла. Примером подобной конденсации может служить получение хинизарина из фталевого ангидрида и гидрохинона  3) Конденсация двух молекул производного оксибензойной к-ты, приводящая вначале также к оксибензоилбензоиной к-те. В отличие от предыдущего, при этом методе ОН-группы могут находиться и при обоих бензольных ядрах антрахинонного цик.та. Примером подобной конденсации может служить получение антрахризона из двух молекул резорцинкарбоновой к-ты HOv COOH ноос- - ~0Н Y СО он 4) Окисление антрахинона и его производных по реакции Бонна-Шмидта. Окисление м. б. проведено либо действием МпОа в сернокислой среде либо серным ангидридом или S2O3B серной к-те в присутствии борной к-ты, азотистой кислоты, серы, селена, брома и т. д. В зависимости от катализаторов, от длительности реакции и температуры ее, при окислении могут получаться различные поли-оксипроизводные, причем ход реакции может контролироваться спектральным исследованием борнокислых эфиров продуктов окисления. А л и 3 а р и н-один из наиболее важных синтетич. красителей, вполне идентичный с естественным ализарином из крапа, корня марены Rubia tinctoria (см. выше, К. в. е с т ес т в е н н ы е); получается он щелочным плавлением ;8-антрахинонсульфокислоты, приготовляемой сульфированием антрахинона (о производстве-см. Ализарин). Плавлением технически чистой /5-антрахинонсульфокис-лоты получают чистый ализарин (синеватый), дающий синевато-пунцовые окраски по алюминиевой протраве. При плавлении в тех же условиях 2, 7-дисульфокислоты антрахинона получается антрапурпурин, дающий по алюминиевой протраве более желтоватые оттенки красного цвета. Желтые оттенки дает флавопурпурин, получаемый при щелочном плавлении 2, 6-дисуль-фокислот антрахинона. Смесь всех трех сульфокислот в различных соотношениях дает ализарин различных марок. Антраруфин и хризазин служат промежуточными продуктами для получения а л и-зарина-сафирола; получают их при сплавлении с Са(0Н)2 соответствующих ди-сульфокислот антрахинона; они не обладают красящими свойствами. Хинизарин, ценный промежуточный продукт для синтеза ряда антрахинонных красителей; он обла- дает весьма слабыми красящими свойствами и получается либо окислением аптрахинона по реакции Бонна-Шмидта, либо конденсацией фталевого ангидрида с гг-хлорфенолом или гидрохиноном в присутствии серной кислоты, причем одновременно с замыканием антрахинонного кольца происходит и гидролиз с отщеплением хлора. Пурпурин получается при окислении по Бонну-Шмидту ализарина или, лучше, хинизарина; мало применим в качестве красителя, служит промежуточным продуктом для получения ализарина сине-черного; сопутствует ализарину в крапе. Антрагаллол получается при конденсации бензойной кислоты с галловой или фталевого ангидрида с пирогаллолом в присутствии серной к-ты. Антрагаллолу может сопутствовать руфигаллол, образующийся при конденсации двух молекул галловой к-ты. Хинализарин, выпускаемый в продажу под названием ализарин-бордо В , содержит ализариновую группировку при одном бензольном ядре и хин-изариновую при другом; получается окислением по Бонну-Шмидту ализарина или хинизарина. Антрахризон, промежуточный продукт для ряда ализариновых (ант-рахризоновых) красителей; получается конденсацией двух молекул резорцинкарбоно-вой к-ты в присутствии серной к-ты и не обладает красящими свойствами. Ализарин-цианин различных марок, смесь пента- и гексаоксиантрахинонов, получается по Бонну-Шмидту при действии дымящей серной к-ты на ализарин, хинизарин, ализарин-бордо в присутствии катализаторов (Н3ВО3, Se, Вт, S, HIslOa); в зависимости от темп-ры, концентрации олеума, катализатора и длительности процесса получаются преимущественно либо пента- либо гекса-оксиантрахиноны. Иногда в реакцию Бонна-Шмидта вводят вместо оксипроизводных антрахинона смесь 1, 5- и 1, 8-динитроантра-хинонов, получая при этом ализарин-цианин WRR; при этом нитрогруппы слулхат одновременно и катализаторами и окислителями. К группе оксиантрахинонов принадлежат также и нитро-, амино- и сульфгидрильные производные антрахинона, как напр.: а л н-зарин оранжевый, или 3-нитро-ализарин, получаемый при нитровании ализарина в ледяной уксусной или в серной кислоте в присутствии борной к-ты, ализарин-цианин G, или 1,2,4-триокси-5, 8-диаминоантрахинон, получаемый при действии 20%-ного раствора аммиака на 1, 2, 4, 5, 8-пентаоксиантрахинон, и ализар и н-м а р р о н, З-амино-1, 2, 4-триоксиантрахи-нон, получаемый при нитровании ализарина в серной к-те и восстановлении полученного при этом З-нитро-1, 2, 4-триоксиантрахино-на. Генетически близко связаны с оксиантра-хинонными красителями и красители типа ализаринового синего, содержащие кроме антрахинонного ядра также и пиридиновое; эти красители получаются из соответствующих аминооксиантрахинонов при действии глицерина в присутствии окислителя и серной кислоты по реакции Скрау-па. В продажу значительно чаще поступает бисульфитное производное ализаринового синего S, Ci7HiiNOioS2Na2 NaOaS-о ОН  SOjNa К-рое весьма удобно для крашения в силу его растворимости в воде. При нагревании выше 60° бисульфитное производное разлагается и на волокне фиксируется яркий и прочный лак красителя с протравой. Бисуль-фитные про изводные в силу это го весьма часто применяются и для иных красителей (напр. церулеиновых и галловых), когда сам краситель плохо растворим в воде. 1 Б. Сульфированные антрахинон. красители содержат сульфогруппу, прочно связанную с ядром красителя и остающуюся в мо.текуле красителя после окраски ткани. Наличие сульфогруппы, повышая кислые свойства красителя, позволяет применять его в качестве собственно кислотного красителя или в качестве хромировочного, если в нем имеются способные к лакообразованию группировки. По способам получения эта группа красителей может быть разбита на два отдела. 1) Аитрахинонные красители, содержащие сульфогруппу в антрахинонном ядре. Простейшим представителем этих красителей является ализариновый красный S, или 3-сульфоализарин, получаемый сульфированием ализарина дымящей серной кислотой при повышенной темп-ре. Аналогичное сульфирование в присутствии ртутн. солей ведет к образованию а-сульфопроизводных ализарина с сульфогруппой в положении 5 или 8, открытых М. А. Ильинским и выпущенных в продажу ф-кой Ведекинда под па-званием эрвеко-кислотный ализариновый красный; полиоксиантрахиноны, как и диоксиантрахиноны, могут давать сульфопроизводные; наибольшее значение имеют аминосульфопроизводные антрахризон а. Кислотный ализариновый синий GR, 4, 8-диамино-2, 6-дисульфокислота антрахризона, получается сульфированием и нитрованием последнего и восстановлением динитропродукта хлористым оловом в кисло11 среде. При восстановлении динитропродукта сернистыми щелочами получается кислотный а л li-зариновый 3 е л е н ы й G, отличающийся от предыдущего наличием двух сульфгид-рильных групп вместо двух амидных. Оба эти красящие вещества являются ценными хромировочн. красителями. Если в приведенных выше случаях вместо антрахризона подвергнуть антраруфин сульфированию, нитрованию и дальнейшей обработке, то по.чу чаются а л и з а р и н - с а ф и р о л, 1, 5-ДИОКСИ-4, 8-диамино-2, 6-дисульфокисло-та антрахинона, и а л и з а р и н-э м е-ральдол, 1, 5-ДИОКСИ-4, 8 дисульфгидро- 2, 6-дисульфокислота антрахинона,-также ценные и широко применяемые кислотные и хромировочные красители. 2) Большое технич. значение имеют аитрахинонные красители, содержащие сульфогруппу в боковой ветви. Общий метод их получения состоит в конденсации аминопро-изводных или оксипроизводных антрахинона с аминами бензольного ряда, анилином, толуидином и др.; в последние сульфо-группа молсет быть введена сульфированием, производимым либо до конденсации либо после нее. Эти красители в зависимости от числа сульфированных ариламидных групп бывают производными моносульфомоноарил-аминоантрахинонов или дисульфодиарилди-аминоантрахинонов; общий скелет первых NH-Аг-SOsNa и вторых NH-Аг-SOjNa NH-Аг-SOsNa причем могут варьировать как положения сульфированных ариламидных групп, так и различные радикалы и ауксохромы в антра-хинонном ядре и в боковой цепи, что вызывает значительное многообразие этих красителей. Из отдельных представителей следует отметить ализарин-иризоль, моносульфокислоту 1-я-то лил амино-4-окси-антрахинона, получаемый при сульфировании продукта конденсации хинизарина с одной молекулой w-толундина. В случае избытка п-толуидина и вторая ОН-группа хинизарина замещается остатком w-толуидина и после сульфирования обоих толуидиновых остатков получается ценный ализарин-цианин зеленый G. При замене хинизарина хинализарином и обработке последнего двумя молекулами w-толуидина, при последующем сульфировании получается ализарин-виридин - протравной и хромировочный краситель. Пурпурин при аналогичной обработке переходит в ализарин сине-черный. Несколько особняком стоит ализарин-рубинол, в котором кроме обычной для этого отдела красителей сульфированной ариламидной группы имеется и пиридоновое кольцо, метилированное при азоте, полученное замыканием из ацетилмонометиламиноантрахинона по следующей схеме СНз /СО N-СНз \ N-CHs \со/ \/\со/ 2 А. Кубовые антрахинонные красители обладают повышенной прочностью к свету, мылу и другим воздействиям; большинство этих красителей получили общее название индантреновых К. в. (см. Индан-трен). По методам получения и свойствам антрахинонные кубовые красители делятся на следующие группы. 1) Ациламиноантрахинонные красители, называемые также альголевыми красителями, представляют преимущественно бензоильные производные различных амино-антрахинонов и получаются при конденсации хлористого бензоила с аминоантрахино- ном в нитробензольной среде. Хлористый бензоил м. б. заменен бензойной и другими ароматич. к-тами-салициловой, и-метокси-бензойной и др. Простейший представитель этой группы - индантреновый желтый WG, 1-бензоиламиноантрахинон. Большое значение имеют полибензоиламиноан-трахиноны: индантреновый красный 5GK-1,4-дибензоилдиаминоантрахи-нон; индантреновый желтый GK- 1,5-дибензоилдиаминоантрахинон, и ряд их окси- и метоксипроизводных. Из трибензо-илтриаминоантрахинонов следует отметить индантреновый оран ж; ев ый RRK, содержащий эти три группы в положениях 1, 2, 4. Ко второй группе относятся антрахинонные кубовые красители, содержащие антрахинонные ядра, соединенные имидными группами,-т. и. антримидные красители. Получаются они гл. обр. конденсацией аминоантрахинонов с галоидоантра-хинонами в присутствии каталитически действующей мелкораздробленной меди (или полухлористой меди) в нитробензольной или нафталиновой среде. Среднее положение между первой и второй группами занимают красители, в к-рых антрахинонные ядра соединены не имидной группой, а карбамидным или имидоянтарным остатками; их получают аналогично альголевым красителям конденсацией двух молекул аминоантрахинона с одной молекулой фосгена или янтарной кислоты; сюда относятся индантреновый желтый 3G, 2, 2- диантрахино-нилмочевина, получаемый при конденсации двух молекул /3-аминоантрахинона с мочевиной или фосгеном в нитробензольной среде, и альголевый желтый 3G, 1,Г-сукцинилдиаминоантрахинон, получаемый при конденсации двух молекул а-аминоан-трахинона с одной молекулой янтарной кислоты в нитробензольной среде -NH-со-NH-\ \со/\/ \/\со/ индантреновый желтый 30 NH-CO-CHg NH-CO-CH2 альголевый желтый 3G 2) У антримидных красителей простейшим представителем является индантреновый оранжевый 6RTK, 1,2-диан-трахинониламин, получаемый при конденсации /3-хлор антрахинона с а-аминоантра-хиноном. Увеличение числа антримидных групп вызывает углубление цвета этих красителей. Так, 2,6-ди-а-антрахинонилдиами-ноантрахинон, полученный при конденсации 2,6-дихлорантрахинона с а-аминоантрахи-ноном, представляет собою индантреновый красный G; его 2, 7-изомер- индантреновый красный R. При введении в эти красители галоидных или метоксильных групп получаются красители еще более глубокого цвета бордо. Триантр-имидные производные, содержащие антра-хинониламиновые остатки в двух а-положе-ниях одного и того же антрахинонного кольца, точно так же являются красителями. Таков индантрен бордо, или 1,5-ди-/5-антрахинонилдиаминоантрахинон, получаемый при конденсации 1,5-диаминоантра-хинона с двумя молекулами хлорантрахи-нона. Весьма интересен факт, что только те антримидные красители являются кубовыми, в к-рых имидная группа соединена с ан-трахинонными ядрами в а-положении с одним и в /5-положении с другим. Так, 1,1ди-антрахинониламин и 1,5-ди-а-антрахинонил-диаминоантрахинон являются окрашенными веществами, но не имеют характера кубовых К. в. Весьма важно и то обстоятельство, что конденсация идет значительно лучше при а-положении амродных групп и при /5-цоложении галоидн. групп, а не наоборот. Арильные остатки в аминоантрахинон-ных производных могут быть также фениль-ными, толильными и нафтильными. Непосредственно подобн. тела не являются ценными К. в.; но если в арильных остатках в о-положении к имидной группе имеются группы, способные к замыканию новых циклов, то такие вещества являются уже ценными кубовыми красителями. Так, наличие группы NHa может привести к дигидроази-новым производным (I), ОН-к оксазино-вым (II), SH-к тиазиновым (III) и СООН- к акридоновым (IV) 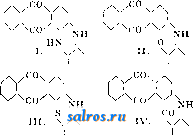 При этом в зависимости от нахождения основной имидной группы в а- либо в /S-поло-Лл:ении м. б. получены различные изомеры. Если имидную группу заменить кислородом или серой, то аналогично м. б. получены ксан-тоны (V), тиоксантоны (VI), диоксаны (VII) и дитианы (VIII) /\/ i I \/\  VII. \/\ VIII. \/\ точно так же с возможными изомерами. Остаток, соединенный с гетероциклом, м. б. фе-ниленовым, нафтиленовым и антрахинони-леновым. Общий метод получения этих красителей может заключаться в конденсации по Ульману галоидоантрахинона с производным амина, фенола или тиофенола и в последующем окислительном, водоотнимаю-щем или крхслотоотнимающем замыкании ге-тероцикла. Для нек-рых отдельных представителей существуют и индивидуальные методы синтеза. 2 Б. Многоядерные красители. 1) К содержащим гетероциклические ядра в первую очередь относится ценнейший индантреновый синий, который кроме получения из двух молекул амино-бромантрахинона, что представляет только теоретич. интерес, получается также и непосредственным плавлением Д-аминоантра-хинона со щелочью. Известен ряд его метиль-ных, окси- и галоидных производных, обладающих несколько измененными оттенками и повышенной прочностью к хлору. Индантрен синий является дигидро (диантралсино-нилен)-азином строения  и относится к производным 1 типа. При более повышенной t° (310°) щелочного плавления у9-аминоантрахинона получается желтый кубовый краситель индантреновый желты й G, или флавантрон, следующего строения  в молекуле к-рого вместо азинового кольца присутствуют два соединенных акридиновых цикла. Красители II и III типа, обладающие оксазиновой или тиазиновой группировкой, не получили широкого применения и представляют в настоящее время лишь теоретич. интерес. Производные IV типа, а к р и д он ы, получили широкое технич. распространение. Простейший из них получается при конденсации а-хлорантрахинона с антрани-ловой кислотой по Ульману с последующим замыканием акридонового цикла при действии конц. серной к-ты. Аналогичная конденсация /9-аминоантрахинона с о-хлорбен-зойной к-той ведет к образованию изомерного акридона. Большую ценность представляют диакридоны, получаемые конденсацией дихлорантрахинонов с антраниловой кислотой, например индантрен фиолетовый RN, имеющий строение HN-I s CO-VcO со--со-1 / И получаемый из 1, 5-дихлорантрахинона. 1 ... 18 19 20 21 22 23 24 ... 49 |
|
© 2007 SALROS.RU
ПромСтройМат |