 |
 |
 |
 |
1 ... 24 25 26 27 28 29 30 ... 48 воде (1 : 7 680). Применяется как белая краска, а также служит для приготовления других М. с. Линолеат марганца,Mn(Cj8H8iOg)8 {часто ошибочно называется олеатом марганца). Получается нагреванием льняного масла с MnOji или с боратом Мп, а также при помощи осаждения раствором MnClj (60 вес. ч. на 150-200 вес. ч. воды) прозрачного мыльного раствора, приготовляемого нагреванием 100 ч. льняного масла с 15 ч. 70 %-ного раствора NaOH, разбавленного 150-225 ч. воды; выпадаюш;ий осадок многократно про-мьшается. Линолеат Мп-аморфная масса, не поддающаяся превращению в порошок. Продажный продукт часто содержит примесь резината Мп. Употребляется как сикатив. Нитрат марганца, азотнокислый марганец, Мп(МОз)2-6 НаО. Приготовляется растворением МпСОз или Мп(0Н)2 в HNO3 или при помощи обработки пиролюзита азотной кислотой в присутствии органических восстановителей (щавелевой кислоты, сахара и т. п.). Бесцветные, исчерченные, расплы-ваюпщеся кристаллы моноклияш. системы, уд. в. 1,8199, растворимые в воде и в спирте. При легком нагревании плавится; кипит при 129,5°, разлагаясь с вьщелением окислов азота и MngOs; в безводном состоянии образует мелкие кристаллы, разлагающиеся при 160-200°. Применяется для изготовления красок для фарфора, при фабрикации анодов из MnOg и как каталитич. удобрение. Оксалат марганца, щавелевокислый марганец, МпСаО*. В бигидратной форме, MnCgOi 2 HgO, он получается из суспензии свежеприготовленного MnCOg в горячей воде прибавлением щавелевой к-ты до кислой реакции. Порошок белого цвета, состоящий из плоских октаэдров, обнаруживающих во влажном состоянии довольно сильную флуоресценщш; постоянен на воздухе. В 1 л воды растворяется при 25° 0,312 г; присутствие оксалата аммония повышает растворимость. Безводный MnCgO* окрашен в розовый цвет; уд. в. 2,4. Бигидрат применяется как превосходный сикатив. Резинат марганца, смолянокислый марганец. В технике применяется 2 вида резинатов: осажденные и сплавленные.Осажденный резинат марганца приготовляется действием горячего раствора MnClg (14,5° Вё) на жидкость, получаемую кипячением смеси канифоли, едкого натра (25° Вё) и воды; осадок отделяют от жидкости, промывают, прессуют, высушивают и измельчают. Осажденный резинат-рыхлый порошок телесного цвета, растворимый в хлороформе, горячем льняном масле и скипидаре. Сплавленный резинат Мп получают сплавлением обезвоженной канифоли с MnOg или же с Мп(0Н)2; поступает в продажу в виде кусков буровато-черного цвета. Резинаты Мп применяются в качестве ценных сикативов. Сульфат марганца, сернокислая закисная соль марганца, MnSOi-n HgO (n= = 0, 1, 2, 3, 4, 5, 7). Встречается в природе в виде маллардита, с 7 мол. воды, и цмикита (шмикита), с 1 мол.воды. Получается б. ч. из природной МпОа. Получение чистого продукта (свободного от солей Fe и др. примесей) достигается лучше все- го прокаливанием MnOg с порошком каменного угля (в пропорции 1 : 10), растворением полученного продукта в HaSO* с добавлением небольшого количества НС1, выпариванием, осторожным прокаливанием для удаления FeS04, выщелачиванием водой и кристаллизацией. Применяются также способы обработки МпОа сперва азотной, а потом серной кислотой или прокаливание пиролюзита с безводным FeS04. Пенгагидрат, MnSOj . 5 HgO, кристаллизирующийся при t° 7-20°, образует бледнорозовые кристаллы триклинич. системы; выше 20° кристаллизуется MnSOi 4 HgO - большие светлоро-зовые моноклинич. призмы; MnSOe 7 HgO выпадает из концентрированного раствора между -4° и -}-6°; MnSOi 3 HgO выпадает вместе с MnS04 4 HgO из кипящего раствора; MnS04 2 н2о пол^ается при плавлении MnSOi 4 н2о или кипячением этой соли со спиртом; при i° ок. 200° перечисленные кристаллогидраты переходят в моногидрат MnSOi HgO. Безводный MnS04 получается нагреванием водных форм до постоянного веса при 280° и имеет вид хрупкой массы с *°ял. 700°, уд. в. 3,282, при сильном накаливании превращаюпщйся в MngOi. Безводная соль гигроскопична и на воздухе постепенно переходит в MnS04 3 HgO; в воде хорошо растворяется (1 ч. на 0,79 ч. холодной и на 1,7 ч. горячей воды); в спирте нерастворима. Растворимость MnSO* 4 HgO в воде (на 100 ч.): при 10 127 4. 37,5 149 Ч. 75° 145 4. 101 92 4. MnSOi легко образует двойные соли, например: K2SO4 MnS04 6н2о; MnS04. А12(804)з- 24HgO и т. д. Сульфат Мп (главн. обр. кристаллогидраты с 5, 4 и 7 мол. воды) широко применяется в крашении и ситцепечатании, а также для приготовления других М. с, в качестве сикатива и каталитич. удобрения. Чистота продукта во многих случаях имеет большое значение (напр. в красильном деле необходимо отсутсгаие соединений Fe). Сульфид марганца, сернистый марганец, MnS. В природе встречается в виде алабандина, марганцевой обманки, марганцевого блеска. Искусственно м. б. получен в модификациях розовато-желтого (телесного) и зеленого цвета. Розовое видоизменение получается действием HgS или сернистого аммония на ще-лочный раствор соли Мп ; зеленый MnS- действием сернистого аммония на кипящий раствор соли Мп . Присутствие MnS сообщает светящижя составам (см.) с основой из серш<[стого цинка способность давать искристую люминесценцию при встряхивании в темноте. Хромат марганца, MnCrOi - см. Хрома соединения и Марганцевые краски. Соли трехвалентного Мп. Соли Мп * образуются при действии НС1 и H2SO4 на холоду на окислы: МП2О3, МП3О4 и MnOg. Очень непрочны и в большинстве случаев могут существовать только при низких (°; при повышении 1° разлагаются; под действием воды они испытывают почти полное гидроли-тич., расщепление. Известны двойные и комплексные соли этого ряда, несколько более устойчивые, чем простые соли Мп . Соли четырехвалентного Мп. Соли Мп чрезвычайно непрочны и едва известны. Только нек-рые соединения, в состав к-рых четырехвалентный Мп входит как часть аниона (т. п. манганиты, напр. СаМпОд), значительно более постоянны. Существование тетрагалогенидов марганца, как MnCli и MnF4, нельзя считать вполне доказанным; однако известны соответствующие им комплексные соединения, которые м. б. также рассматриваемы как соли кислот HgMnClg и HgMnFg. К соединениям Мп относятся также: КИСЛЫЙ арсенат марганца, MnCHaAsOi) довольно устойчивый в растворах, дисульфид марганца, MnSg, встречающийся в природе в виде г а у ер и т а, и манганиты кальция (СаМпОз и СаМПаОз), образующиеся при смешивании гашеной извести с раствором MnClg и продувании через эту смесь воздуха. Все манганиты являются солями гипотетических кислот состава НаМпОз (или HjO MnOg), HMnO, (или 2 HjjO MnOa) и Н2МП2О5 (или HgO 2МПО2); окислы МПаОз и МП3О4 также иногда рассматриваются как марганцевые соли этих к-т: МпМпОа (или MnO-MnOg) и МП2МПО4 (или 2 МпО МпОа). Соли марганцовистой кислоты, м а н г ан а т ы. Эти соли получаются сплавлением окислов Мп или его солей со щелочами и щелочными со.тями в присутствии воздуха или каких-нибудь окислителей, напр.: 2Ме2С0з + 2Мп02 + Оа =2Ме2Мп04 + 2CO2. манганат Манганаты могут существовать лишь в присутствии свободной щелочи; прибавление кислот, даже слабых, или избытка воды ведет к быстрому гидролизу соли, сопровождаемому переменой валентности Мп, в результате чего получаются щелочь, МпО а и соль марганцевой к-ты. Манганат бария, марганцовистоки-слый барий, BaMnOi. Получается слабым прокаливанием MnOg с Ва(0Н)2 или же с BaC08-l-Ba(N08)a (последняя соль служит окислителем). Изумруднозеленый микро-кристаллич. порошок, уд. в. 4,85, нерастворимый в воде. Применялся как краска под названием кассельской, марганцевой или баритовой зелени, заменявшей более ядовитую швейнфуртскую зелень. Манганат калия, марганцовис-токислый калий, минеральный хамелеон , К2МПО4. Образуется при сплавлении МпОа и КОН в присутствии окислителей или при хорошем доступе воздуха. Сплав, содержащий К2МПО4, получается в качестве промежуточного продукта при производстве пер-манганата калия. Тонкоизмельченная порошкообразная МпО а сплавляется в котлах с едким кали крепостью в 50° В6, причем массу тщательно перемешивают во избежание спекания в комья; наиболее благоприятная t° = 250°; процесс длится 10-12 час. В результате этой плавки значительная часть Мп остается неокисленной; поэтому после измельчения плава на шаровых мельницах производится его обогащение в особых снабженных мешалками котлах, где порошкообразная масса подвергается продувке горячим воздухом. При употреблении для этой цели спещ1альных печей Шютца про- цесс обогащения заканчивается в 2-3 часа. При фабрикации КМПО4 полученный по описанному способу продукт подвергается дальнейшей переработке (см. ниже перманга-нат калия). При растворении содержащего КМПО4 плава в воде получается жидкость темнозеленого цвета, из которой при испарении в вакууме выделяются зеленые приз-матич. кристаллы безводной соли К2МПО4. В отсутствии избытка щелочи раствор К2МПО4, особенно в разбавленном состоянии, при соприкосновении с воздухом постепенно изменяет свой цвет из зеленого в малиновый, вследствие чего К2МПО4 и был назван минеральным хамелеоном; при этом происходит образование KMnOi и выпадение MnOg. При действии перегретого водяного пара KaMnOi образует МП2О3, КОН и свободный кислород, а при нагревании твердого остатка в струе воздуха он вновь переходит в К2МПО4; этот процесс предлагался как способ технич. получения кислорода. К2МПО4 является довольно сильным окислителем. Манганат натрия, марганцовисто-кислый натрий, NaMnOi. Получается в технике путем сплавления 1 ч. пиролюзита, содержащего ок. 40% Мп, с 1,44 ч. NaOH или с 1,1 ч. NaOH-f 0,4 ч. KNOg: 2KN03+2Mn02-b4N£0H=2Na2MnG4+2KN02+2H2O. Сплавление производится в муфельной печи, нагреваемой (если процесс ведется без селитры) перед наполнением до 450°. Затем Р постепенно повышают до 500° и поддерживают на.этом уровне 8 час. Охлажденный продукт (содержащий ок. 28% манганата) идет неносредственно для практич. применения (см. также ниже-перманганат натрия). Из водного раствора соли м. б. вьщелены темнозеленые кристаллы состава NagMnOi 10 НаО. Получаемый вышеуказанным способом сырой продукт отличается дешевизной и применяется в качестве дезинфекционного средства, в цианистом процессе извлечения золота, а также в различных окислительных процессах лабораторной и производственной практики. Соли марганцевой кислоты, перманга-наты. Эти соли получаются способами, сходньпли со способами получения мангана-тов. Наибольшее значение в технике имеют способы, сводящиеся к гидролизу предварительно полученных манганатов. В последнее время преимущественное значение приобрели электролитич. методы получения перманганатов из растворов манганатов. Все перманганаты в твердом виде-темно-фиолетовые кристаллы, дающие интенсивно окрашенные малиново-красные или фиолетовые растворы; почти все они (за исключением AgMn04) хорошо растворимы в воде. В химич. отношений перманганаты характеризуются как весьма энергичнью окислители. Выделение из них кислорода происходит уже при нагревании сухой соли, напр. 2КМп04= К2Мп04 + Мп0а+ О2. Окисление перманганатами в растворах протекает в кислой и щелочной среде различно. В присутствии щелочи сначала выделяется 1 атом кислорода из каждых 2 молекул пер-манганата, напр.: 2КМп04 + 2К0Н=2К2Мп04 + Н20+ о. затем образовавшийся манганат в свою очередь разлагается: 2К2Мп04 + 2Н20 = 2МаОа+4КОН+20. Окончательно окислительное действие пер-манганата в щелочном (а также в нейтральном), растворе отвечает следующему ур-ию: 2 KMaOi + НаО = 2 MnOg + 2 КОН + 3 О, Т. е, 2 мол. перманганата отдают 3 атома кислорода. Окисление перманганатом в кислой среде м. б. изображено напр. следующим образом: 2КМПО4+П2804 = K2SO4 + 2ИМПО4; 2HMnG4 + 2H3S04 = 2MnSOi + 3HaO +50 или окончательно: ЗКМпО* + 3H2S04= K2SO4 + 2MnS04 + 3H2O + 5 о, т. е. 2 мол. перманганата отдают 5 атомов кислорода. Перманганаты находят широкое применение как окислители в самых разнообразных лабораторных и производственных процессах. Перманганат алюминия, марган-цевокислый алюминий, А1(Мв04)8. Приготовляется действием 53 частей КМПО4 при нагревании на 1 ООО ч. раствора, содержащего Vs А12(804)з по весу. После охлаждения вы-кристаллизовьшаются алюминиевые квасцы, от к-рых декантацией отделяется раствор, содержащий перманганат алюминия и значительное количество Al2(S04)8. Этот раствор употребляется непосредственно для дезинфекции и других целей. При окислительных реакциях перманганат А1 отдает своего кислорода. Перманганат калия, марганцево-кислый калий (иногданеправильно называется хамелеоном), КМПО4. Для получения его было предложено много способов. Совершенно чистый KMnOi м. б. получен: а) путем выпаривания досуха смеси 8 ч. MnOg и 7 ч. KCIO3 с крепким раствором 10 ч. КОН, измельчения полученной массы, нагревания порошка ок. 1 ч. при тёмнокрасном калешпг до полного разложения KCIO3, извлечения темнозеленого плава кипящей водой при кипячении, фильтрования раствора через асбест и быстрого выпаривания до кристаллизации или б) электролизом раствора щелочи с анодом из ферромарганца. Технически КМПО4 получается б. ч. из манганата KaMnOj. Превращение последнего в перманганат м. б. достигнуто действием хлора: 2 KaMnOi + GI2 = 2 КС1 + 2 КМпО*. Действие сульфата магния на К2МПО4 также приводит к образованию перманганата: 3KaMn04 + 2MgS04 + 2HaO =2КМп04 +2K2SO4 + + 2Mg(0H)a + Mn02. До недавнего времени на з-дах предпочитался способ обработки раствора манганата, полученного по описанному выше методу (см. выше-манганат калия), углекислым газом при t° 40-60°. В настоящее время в крупных производствах применяются исключительно электролитич. способы получения перманганата из раствора манганата; из них наибольшее распространение получает без-диафрагменный способ Э. Шютца Р]. Согласно этому способу плав, содержапщй манганат калия, растворяется при 40° в жидкости, представляющей профильтрованные остатки от предыдущего электролиза, разбавленные промьшными водами от промывания кристаллов; ее крепость должна составлять 25° Вё. Растворение производится в сосудах с мешалками. В раствор переходят KgMnOi и КОН, причем вьщеляется некоторое количество регенерированной MnOg, которая отделяется декантацией. Раствор с уд. в. около 1,4 фильтруется и подвергается электролизу в цилиндрич. железных ваннах с конич. дном, снабженным спускными кранами. Внутри ванн находятся приспособления для перемешивания электролита, а также никелевые аноды и железные катоды, поддерживаемые стеклянными изоляторами, прикрепленными ко дну ванны на цементе. Каждая ванна вмещает 960 л жидкости (до уровня 20 см от ее верхнего края). Темп-ра электролиза 30-60°, плотность тока 30- 40 А/дм прл напряжении 25-27 V. Процесс продолжается 10-11 ч. и идет по ур-ию: 2К2Мп04+2На0 =2КМп04 + 2К0Н + Н2. О его окончании судят по цвету пробы, взятой на стекло. Для месячной продукции ок. 10 ш КМПО4 необходимо иметь 16 ванн. В качестве побочного продукта при электролизе образуется нек-рое количество MnOg, к-рую необходимо периодически тщательно удалять, т. к. она каталитически ускоряет разложение манганата и перманганата. Вся смесь, получаемая в результате электролиза, переводится в кристаллизационные чаны и охлаждается водой или водой со льдом; выделившиеся кристаллы перманганата отделяются от маточного рассола центрифугированием, промываются малым количеством холодной воды, высушиваются в вакууме и пропускаются через шаровую мельницу. Полученный продукт содержит 99% КМПО4. Маточный рассол снова идет в производство, а по накоплении в нем значительных количеств карбонатов подвергается каустизации, для чего его сгущают выпариванием до уд. в. 1,32, отделяют от выпавших перманганата, манганата и MnOg; затем разбавляют до уд. в. 1,1, обрабатывают едким кали и снова сгущают до уд. в. 1,5. Перманганат калия- хорошо образованные красно-фиолетовые, почти черные ромбич. призмы с зеленоватым металлич. блеском; уд. в. 2,71. Растворимость (в 100 ч. воды): при -0,58° 4° 10° 20° 30° 40° 60° 70° 75° 3,0 3,36 4,4 6,51 9,06 12,53 21,99 28,6 32,35 Раствор КМПО4 В воде нейтрален: окраска его еще видна (в слое в 20 см) при 1 ч. соли в 500 ООО ч. воды. КМПО4 растворяется также в ацетоне, уксусной к-те, пиридине, метиловом спирте. КМПО4-один из сильнейших и наиболее употребительных окислителей. При нагревании до 200-240° он выделяет кислород, сильно разогреваясь; при растирании его с серой или фосфором происходит взрыв; многие органич. соединения воспламеняются им при нагревании, а некоторые (напр. глицерин)-и при обьпсновенной t°. Не вполне чистые растворы КМПО4 постепенно разлагаются (особенно на свету) с выделением MnOa-aq; поэтому их следует хранить в сосудах из темного стекла со стеклянными пробками. Растворы КМпО* разрушают бумагу и ткаш1; поэтому их филь- труют через асбест или стеклянную вату. Концентр. НС1 окисляется перманганатом на холоду, разбавленная-при нагревании, с выделением хлора (удобный лабораторный способ получения хлора). Раствор КМПО4, особенно подкисленный, быстро восстанавливается сернистой кислотой и ее солями, закисными солями железа и другими восстановителями, причем получаются соли Мп . Цинк, железо, свинец, ртуть и многие другие металлы б. или м. быстро окисляются растворами КМпОд, На окислительной способности КМПО4 основаны почти все случаи его практич, применения. В виду того что реакции окисления им протекают строго количественно и сопровождаются резким изменением окраски раствора, КМПО4 применяется в количественном (объемном) и качественном хим. анализе. В препаративных и производственных химич. процессах применение КМПО4 как окислителя весьма разнообразно. Он употребляется в органич. синтезах, при изготовлении сахарина, в цианистом процессе извлечения золота, для отбелки и обесцвечивания волокнистых материалов, эфирных масел, жиров и восков, для очистки газов, в ситцепечатании, для окрашивания дерева в коричневый цвет, в составе смесей для фотографич. вспышек, в медицине и санитарии как стерилизуюш;ее средство и т. д. Хороший препарат перманганата калиядолжен удовлетворять следющим требованиям. 1) 0,5 г КМПО4 доллшы давать бесцветный фильтрат после кипячения со смесью 2 см винного спирта и 25 сл*з воды; этот фильтрат после прибавления 2 см HNO3 (уд. в. 1,15.Я) должен давать в крайнем случае только слабую и-гуть с Ва(К0з)8 и с AgNOs (проба на сульфаты и хлориды). 2) Если в раствор 0,5 г КМПО4 в 5 см воды, нагретый до 50-60°, постепенно ввести 1 г кри-сталлич. щавелевой кислоты, то смесь 2 слеЗ профильтрованного раствора с 2 см серной к-ты при соприкосновении с раствором FeS04 не должна давать темного кольца (проба на нитраты). 3) Нагрев 2 г КМпО, в платиновом тигле, вносят кусочки парафина до тех лор, пока не перестанут происходить вспышки; охла-нвденный остаток выщелачивают водой, фильтруют и бесцветный фильтрат обрабатывают 6 сл з азотной ки--слоты (уд. веса 1,153). После прибавления раствора AgNOs жидкость должна оставаться прозрачной или обнаруживать только слабую опалесценцию (проба па хлораты). Перманганат кальция, марганце-вокислый кальций, Са(Мп04)г-5НаО,-см. Жальция соединения. Перманганат натрия, марганце-вокислый натрий, NaMn04 ЗНО. Вследствие технич. затруднений, встречающихся при изготовлении этой соли в чистом виде, ее получают б. ч. в смеси с манганатом. Способы получения в общих чертах сводятся к нагреванию MnOj со смесью едкого натра -с бертолетовой солью или селитрой и к извлечению смеси манганата и перманганата натрия водой. Обыкновенно смесь манганата и перманганата натрия приготовляют, сплавляя МпОа с каустической содой в течение 48 ч. при t° тёмнокрасного каления; полученная масса выщелачивается водой, декантируется, и раствор окисляется до требуемой концентрации NaMnOi. При необходимости получить продукт, состояпщй из од-яого перманганата, маточный раствор обра- батывается HaS04 и вьшаривается до выделения кристаллов N32864. Перманганат натрия-распльшчатые, легко растворимые в воде кристаллы; по своим свойствам он очень похож на перманганат калия и может применяться в тех же случаях, как и последний. Однако трудность получения в чистом виде препятствует его техшч. применению в широких размерах. Соединения Мп неопределенной валентно-сти. Сюда относятся след.: антимониды марганца, MnSb и MnSbg, а также Шщ8Ь и MngSba; арсениды марганц а-MngAs (наиболее устойчивый), МпзЛза и MnAs (устойчив только в пределах 400-450°); бо-риды марганца - МпВ и может быть MnBg; карбид марганца, МпдС; нитриды марганца-MngNa, MngNg и м. б. MhtNs; силициды марганца-MngSi, MnSi, MnSia и м. б. MngSij; фосфиды марганц а-МП5Р2, МП3Р2 и МпР. Большинство перечисленных соединений обладает магнитными свойствами; технич. значения они пока не имеют. Аналитическое определение Мп в М. о. Качественные реакции. 1) При сплавлении М. с. с содой и селитрой образуется сплав зеленого цвета (чувствительность-0,005 мг Мп). 2) Перл сплавленной фосфорнокислой соли или буры в присутствии М. с. окрашивается в окислительном пламени в аметистовый цвет; в восстановительном пламени происходит обесцвечивание. 3) Разбавленный раствор солп Мп после окисления азотной к-той при кипячении и прибавления РЬОа приобретает красно-фиолетовую окраску, вследствие образования НМПО4 (чувствительность-0,002 мг Мп; хлористые соли мешают реакции). 4) Для открытия очень малых количеств Мп в почве, минералах, золе растений и животных и т. п. реакция (3) видоизменяется т. о., что окислителем, вместо РЬОг, служит персульфат аммония в присутствии 1 капли раствора CoCNOsb- 5) Очень чувствительным реактивом на М. с. (в отсутствии Си и РЬ) является тетра-фенилдиаминодифенилметан, дающий после сплавления пробы с NaOH я подкисления уксусной к-той при нагревании синее окрашивание. 6) Соли Мп м.б. открыты в 0,0001 JV растворе по красному окрашиванию с 0,1 N раствором К JO*. 7) Манганаты и перманганаты легко открьгааются благодаря их способности менять цвет при окислительных и восстановительных реакциях. Количественное определение. Весовое определение Мп производится обыкновенно путем перевода его соединений в МП8О4: отделенный от других металлов Мп осаждают содой при кипячении, осадок МпСОз прокаливают и взвешивают. Объемный метод, годный для определения небольших количеств Мп (при отсутствии хлоридов), заключается в окислении пробы при помощи PbOa-bHNOs, удалении РЬ в виде PbS04 и горячем титровании Мп раствором щавелевой н-ты (или раствором мышьяковистокислого натрия, или переквш>ю водорода). Удобный способ объемного определения Мп, предложенный Фольгар-дом и Вольфом, основан на том, что соли Мп в присутствии ZnO количественно окисляются перманганатом в МпОа и переводятся ZnO в манганит цинка: 8MnCla + 2КМПО4 + 2 НаО = 2KG1 -h 4HC1 + бМпО или схематически: ЗМпО + Мп207 = 5Мп02. Согласно варианту метода, предложенйому Фишером, исследуемая руда или сплав (1 г) растворяется в царской водке, выпаривается почти досуха; остаток растворяют в 300 смз воды, смешивают с эмульсией окиси цинка и доводят до 1 л. Отобрав 100 сив раствора, разбавляют до 500 см , вносят 10 ч. ZnS04 и нагревают до кипения; затем прибавляют 1 ч. свежепрокален-пой окиси цинка и титруют 0,1 N раствором КМПО4 при кипячении до покраснения раствора: пост этого прибавляют 1 см уксусной кислоты (причем окраска исчезает) и титрование перманганатом медленно доводят до конца в горячем, но не кипящем растворе. Оценка пиролюзита в смысле содержания деятельного кислорода производится след. обр.: измельченная проба пиролюзита просеивается и высушивается до постоянного веса при 105°; из нее отвешивают 5 г и нагревают их с 50 са титрованного раствора FeSP4 до растворения; раствор разбавляют примерно до 15и сд! и избыток Fe оттитровывают перманганатом. Лит.: 1) Г. П. 195524; ) Г. П. 327086/1919; ) .Z, angew. Ch. , 1911, 24, p. 1628,630; Ch. T ., 1911, химии, гл. 21, М., 1924; О с т Г., Химич. технология, пер. с нем., вып. 2 и 4, Л., 1927; Смит А., Введение в неорганич. химию, пер. с англ., вып. 2, М.-Л., 1929; Цинберг С. Л., Руководство по химич. анализу в металлургич. производстве. Л., 1929; Ull-inanns Enzyklopadie, В. VlII, p. 9-25; К a t о J. a. M a t s u h u s i Т., Journ. See. Chem. Ind. of Japan , 1929, v. 32, и (получение MnOg); E p h г a 1 m F., Anorgan. Chemie, 4 Aufl., Dresden-Leipzig, 1929; T h 0 г p e В., A Dictionary of Applied Chemistry, vol. 4, p. 210-218, London, 1928; Handb. d. anorgan. Chemie, hrsg. v. R. Abegg und Fr. Auerbach, B. 2, Abt. 2, Leipzig, 1922; G m e li n-K r a u t, Handb. d. anorgan. Cliemie, Heidelberg, 1905-16. B. Горшешников. МАРГАНЦЕВЫЕ КРАСКИ вырабатываются из солей закиси и окиси марганца в смеси с углекислыми солями натрия, бария и фосфорной кислоты. Цвет красок получается -белый, зеленый, коричневый и черный в зависимости от тех соединений, с к-рыми соли марганца вступают в реакцию. Марганцевая белая, углекислый марганец, MnCOg, получается из растворов MnClg и NagCOs; нежный белый порошок, уд. в. 3,13. Чисто белый осадок вьшадает лишь только в том случае, если к раствору MnClj прибавить сначала небольшое количество NagCOg для удаления примеси железа, к-рая придает белому осадку грязноватый тон. После отстаивания и отделения осадка к жидкости приливают остальное количество соды (избегая ее избытка) и получают осадок совершенно белого цвета. Высушенный и промытый осадок идет как масляная и акварельная белая краска в живописи. Марганцевая коричневая, марганцевый бистр, вырабатывается из природной желтой железной руды, содержащей до 50% перекиси марганца. На красочные з-ды масса доставляется в сыром виде, где ее высушивают и обжигают, причем в зависимости от t° обжига и чистоты исходного материала получаются различные сорта по тону и качеству краски. Марганцевый бистр приготовляется также и искусственным путем <см. Бистр). Марганцевая коричневая имеет применение в обойном и типографском деле, в живописи, при приготовлении темных олиф, а также в крашении тканей (см. Крог шенш минеральными красками). При приемке М. к. исследуют на цвет и кроющую способность. При кипячении проба краски с соляной кислотой не должна обнаруживать шипения, что указьшает на примесь мела, а при нагревании со щелочью но датжна окрашиваться в бурый цвет. [Марганцевая зеленая, манганат бария-см. Марганца соединения. Существует несколько способов ее приготовления, каждому из них соответствует определенный оттенок и определенная стойкость к атмосферным влияниям. На красочных з-дах марганцевую зелень получают из 14 ч. окиси марганца, 80 ч. азотнокислого бария и 80 ч. тяжелого шпата. Нагрев ведут до тех пор, пока не получится желаемый тон; затем массу подвергают разМолу, промьшают и сушат. Высшие сорта марганцевой зелени получают по двум способам: Розенштиля и Бетгера. Первый способ состоит в быстром' смешивании 4 ч. едкого бария и 2 ч. азотнокислого бария с 0,5 ч. окиси марганца. Смесь слегка смачивают водой, после чего нагревают до тёмнокрасного каления. Расплавленную массу бросают в воду, выщелачивают и затем сушат в особых аппаратах в присутствии едкой щелочи, что способствует получению продукта, свободного от углекислоты, красивого зеленого цвета. При этом способе надо иметь в виду, что, чем больше было взято с^гхого бария, тем ярче получается оттенок краски. Для получения темнозеленого тона краски осадок варят со слабой НС1. Способ Бетгера состоит в прокаливании смеси MnCla с 2 ч. перекиси марганца. Оба вещества смешивают в хорошо истертом виде и смесь нагревают до плавления, после чего ее обрабатьтают водой. Полученный раствор смешивают с раствором соли бария. Образующийся осадок имеет фиолетовый тон; его промывают, сушат и растирают с 1 частью едкого натра. Смесь медленно нагревают до красного каления-до приобретения зеленого цвета. Процесс надо вести медленно, т. к. в противном случае начнет выделяться хлор и осаждаться перекись марганца, придавая краске черный цвет. Применяется марганцевая зеленая гл. обр. в живописи, так как она очень стойка и красива. В торговле под видом марганцевой зелени продается краска, к-рая вырабатывается из сернокислого марганца и углекислого натрия. Осадок прокаливают в тигле без доступа воздуха, что достигается опусканием тигля со смесью в другой тигель, наполненный мелким древесным углем. Краска по цвету и стойкости хуже манганата бария, но дешевле. Применяется она для окраски металлов. Марганцевая фиолетовая получается плавлением перекиси марганца с фосфорной к-той; состав ее точно не определен, вероятнее всего-метафосфат марганца. Расплавленную массу вываривают в растворе углекислого аммония и, отфильтровав осадок, вновь прокаливают; после промьшки получают осадок красно-фиолетового цвета. Если хотят получить краску с голубоватым оттенком, то при первой плавке прибавляют небольшое количество соли окиси железа. Марганцевая фиолетовая имеет незначительное применение как малярная краска в живописи. Марганец входит также в состав умбры (см.). с, Михайлов. Лит.: СМ. Краски минеральные. МАРГАНЦЕВЫЕ РУДЫ широко распространены в природе и встречаются во многих странах в месторождениях осадочного характера-пластовых, жильных, гнездовых и россьшных. Месторождения промьппленно-го значения однако не столь многочисленны. Минералы, содержахцие марганец, приведены ниже в таблице. Главнейшими минералами, образующими залежи М. р., являются следующие: имро-люзит (см.), манганит, браунит, псиломе-лан, родохрозит, родонит (см.), вад (см.), полланит, гаусманит (см.), гауерит, марганцевый блеск. М. р. в большинстве месторождений залегают совместно с минералами, образующими железные руды, и потому, в зависимости от количественного содержания и преобладания в руде железа илИ марганца, нередки переходные стадии в виде руд железо-марганцевых и марганцево-железных. Минералы, содержапще марганец, служащие для извлечения содержапщхся в них сереб- Минералы, содержащие марганец. Минералы Крист. сист. Мп, % Уд. вес Марганцевый блеск (ала- бандин)........... Куб. Гауерит........... Канеит........... (?) Манганозит........ . Куб. Браунит........... Тетр. Пиролюзит (черный марганец)............. Ромб. Полианит.......... Тетр. Гаусманит.......... Якобсит........... Куб. Франклинит ........ Креднерит......... Моеок.ч. Пирохроит......... Геке. (Триг.) Манганобрусит....... Геке, Манганит.......... Ромб. Халькофанит........ Геке. Псиломелан......... - Вад............. - Марганцевый шпат (родохрозит) ...........i Геке. (Триг.) Манганокальцит...... Ромб. Илезит........... - Фозерит........... Ромб. Маллардит......... Монокл. Гюбжерит.......... Вольфрамит......... Литиофиллит........ Ромб. Дикйяябонит........ Моноил. Файрфильдитр........ Трикл. Реддингит.......... Ромб. Гетерозит......... . Монокл. Гюролит........... Триплоидит......... Эосфориг.......... Ромб. Тефроит ........... Кнебелит.......... Гидротёфроит........ - Спвссартин (гранат) .... Куб. Гельвин........... фриделит.......... Геке. (Триг.) Кремнистый марганец (го- донит, орлец)........ Трикл. Гидрородонит........ Кентролит......... Ромб. MnS MnSs МПщАвп МпО МпаОв МпОа МпОа МпзО* MnO(Fe2 , Мп2)Оз (Zn, Fe, Mn)(Fea, Mu2)04 2МпаОз 3 CuO MnOHaO (Mg, Mn)0 HaO МпаОз-НаО (Mn, Zn)0-2MnOa 2 HaO 4MnOa-RO-H20 *i Mn02(Mn, R)0 xHaO а MnCOa МпСОз(Са, Mg)C03 (Mn, Fe, ZtOSO* 4H2O (Mn, Mg)S04 5 HaO MnS04-7H20 MnOWOs (Mn, Fe)W04 LiaO 2MnO-?a05 4{Mn, Ca, Fe, Na2)(P04)2 3 HgO 2CaO.MnO.PaO5 - 2HsO MnO P Qs - 3 HaO H(Be, Mn)4(?04)8 (Mn, Fe)0 . P2O5 5 HgO 4(Mn, Fe)O.PaOsHaO 2 MnOAlaOg PaOs 4 HjO 2 MnO SiOa 2 (Mn, Fe)0Si02 2 MnO-SiOa X H2O 3 MnO-AlaO 3- 3 SiOa (Mn, Be, Fe), SigOiaS (Mn, Fe)0 8 SlOa MnCla 7 HgO MnO SiOa MnO-SiOa xHgO 2 МП2О3 3 PbO 3 SiOa 63,2 46,1 (?) 77,5 69,6 63,2 63,2 72,0 16,6-21,5 5,4-13,4 39,7 61,8 I 60,4 i49,2-62,9 47,8 52,3 17,9 15,2-15,5 19,8 18,3 3,7-17,2 35,0 18,6-1! 15,2 #.3 13,5 31,7 37,5 18,2 54,4 27,1 83,3 27,3-38,1 39,8 41,9 15,1 3,5- 4 5 (?) 6-6 6-6,5 2-2,5 6,0-6,5 5-5,5 6 6,0-6,5 4,5 2,5 2,5 5-6 1-3 3,5-4,5 4-5 2-2,5 4,5 5-5,5 4,5 3,5-4 3,5 3~вуб 4,6-5,6 3,5 4,5-5 5,5-6 6-6,5 4 7-7,5 6-6,5 4-5 5-5,5 5-6 5 3,9-4,1 5,2 4,7-4,9 4,8-5 4,8-5,0 4,7-4,8 4,7 5,0-5,1 4,2-4,4 3,9 4,1-4,3 2,3-3,7 3,3-3,6 ,3,0 7,1 7,1-7,5 8,iS 3,1 3,4-3,5 3,13 3,9-4,2 3,1-3,3 4,1 3,7-4,4 3,1-3,3 3,5-3,7 2,7 6,16 *i R=Ba, Ka, Lig. *2 R=Ba, Ca, K2. pa, цинка, свинца, причисляются к рудам этих металлов, что не исключает возможности использовать эти руды и для извлечения марганца. Усиленное развитие добычи, псугребления и международной торговли М. р. возникло во второй половине прошлого века, когда М. р. нашли широкое применение в металлургии при производстве стали и выплавке марганцевых соединений железа (зеркальный чугун, ферроманган), отчасти и сплавов с цветными металлами. В настоящее время для указанных надобностей идет более 90% мировой добычи М. р. Остальные 10% находят применение в производстве сухих электрических элементов, в стекольной промышленности, в приготовлении марганцевых препаратов, применяемых в химической промышленности, в производстве красок, при получении хлора и родственных ему элементов, также для медицинских целей, дезинфекционных средств и др. Одна из разновидностей марганцевых руд, родонит, или орлец, применяется в качестве поделочного камня, а также в строительном деле для облицовок. Мировые запасы М. р. по наличным данным исчисляются свыше 500 млн. т, из них в СССР более 210 млн. т, в Брит. Индии более 100 млн. ш, в Бразилии 140 млн. шив африк. месторождениях свьппе 40 млн. т. Запас прочих стран, в том числе США, Испании, Великобритании, Германии, Франции, Бельгии, Румынии и др., сравнительно невелики, а запасы Японии и Китая мало известны. Несколько более значительными запасами обладаш повидимому Австралия. Месторождения М. р. Брит. Индии обнаружены по всей стране, наиболее богатые- в центральных районах. Нек-рые из них значительных размеров (по простиранию до 2,5 км и мощностью до 30 м сплошной руды, преимущественно псиломелана и браунита, реже пиролюзита и др., с содержанием 46-56% Мп, 4-9% Fe, 5-7% SiOg и ~0,1% Р) удобны для разработки открытыми работами, но удалены от моря. Бразилия обладает значительными месторождениями М. р., весьма пригодных для металлургич. целей, с содернсанием 44-;58% Мп, 1-7% Fe, 0,01-0,2% Р, до 14% SiOa, немного AI2O3. Из африк. месторождений М. р. наибольшее значение имеют месторождения Золотого Берега с высокопроцентной рудой, гл. обр. псиломелана, пиролюзита, манганита и полианита, среднего состава 42-53% Мп, 2-4% Fe, 3-7% SiOa, 0,1-1,12% P.- В Ю.-Африканском союзе преобладающее значение имеет открытое в 1925 г. близ Пост-масбурга месторождение, представляющее плотный, в небольшой части грубокристал-лич. псиломелан, с запасом более 18 млн. w, пласт, мощностью до 6 л , с содержанием 42-58% Мп, 3,25-10% Fe, 1,75-7% SiOa, при отсутствии Р; пласт частично залегает на поверхности и доступен для эксплоатации открытыми работами. Приобретают также значение месторождения железо-марганцевой руды в Египте, на Синайском полуострове. Руда нуждается в обогащении, содержит (в среднем из 211 анализов ) 32,36% Мп, 25,08% Fe, 2,79% SiOa, 3,29% BaSOj, 0,126% P. Главнейшим месторождением М. p. мирового значения в СССР является Чиатурское, в Шорапанском. районе Грузии (соединено ж. д. длиною 165 км с морем), с запасом свьппе 65 млн. т руды, преимущественно пиролюзита и манганита, с содержанием40- 50% Мп, - 1,5% Fe, 9% SiOg, до 0,2% Р, ~2% СаО. Пласт залегает почти горизонтально, мощностью в среднем не менее 2 м. Примерно рудного запаса м. б. использована без обогащения, а */з путем промывки легко м. б. доведены до содержания 52- 56% Мп. Разработка производится штольнями шириною до 4 j№ по выходам руды на поверхность. Прочие месторождения Грузии не разрабатьшаются и не имеют пока особенного значения. Вторым по значению месторождением М. р. в СССР является Никопольское на Украине. Толщина рудного слоя 1-1,5 м, достигает в нек-рых местах 3,5 м. Запас М. р. исчисляется в 75 млн. т пиролк ита с содержанием 28-33% Мп, до 25% SiOj, ~0,2й% Р. Руда требует предварительной промывки. В обогащенной руде содержится 42-52% Мп, 0,3-0,7% Fe, 0,17- 0,3% Р, 8-16% SiOg. В виду гнездового характера рудных стяжений и неглубокого залегания пласта разработка ведется небольшими шахтами сроком службы 2-3 года. Значительные запасы М. р. обнаружены в МангЫшлакском месторождении Казакской АССР и Лабинском-на С. Кавказе. Запасы первого исчисляются в 33 млн. ш 22%-ной руды и второго-в 34 млн. ш весьма кремнистой руды с содержанием 7-53% Мп. Про-мьппленное значение обоих месторождений зависит от изыскания способов экономически выгодного обогащения руд этих месторождений. Прочие месторояедения М. р. в СССР, в том числе месторождения уральские,-преимущественно местного значения. Мировая добыча М. р., постепенно увеличиваясь в течение нескольких десятков лет, достигла в 1913 г. максимума в 2 300 723 т. Первенствующей по добыче являлась преимущественно Россия, добывшая в 1913 г. 1 245 288 т (965 848 т-Чиатуры, 275 864 т Никополь, 3 576 т-Урал). С нею в нек-рые годы успешно конкурировала Брит. Индия. Война 1914-18 гг. и последующая революция вызвали снижение мировой добычи М. р., обусловленное гл. обр. сокращением добычи в СССР, снизившейся в 1921 г. до 11 952 т. С этого года мировая добыча постепенно восстанавливается и, превзойдя в 1925 г. рекордные цифры 1913 г., достигла в 1926 г. 3 208 569 т. Первенство по размерам добычи принадлежит Брит. Индии (в 1927 г.- 1 147 479 т), вторым следует СССР, добыв- ший в 1927 г. 843 850 т, причем общая добыча этих двух стран составила в 1926 г. 64,2 % всей миршой добычи (в 1913 г.-90 %). Третье место в мировой добыче, принадлежавшее Бразилии, занял в последние годы Золотой Берег (Африка), добывший в 1927 году 4.50 ООО т. Бразилия с добычей в 1927 г. 241 823 т перешла на четвертое место. Малопроцентные руды железо-марганцевые в значительных размерах добываются в Германии (в 1927 году 189 176 т с содержанием 12-30% Мп) и США (в 1927 году 136 151 т с содержанием 10-35% Мп). Добыча М. р. в остальных странах сравнительно невелика, и лишь Чехо-Словакия в 1927 г. достигла добычи 108 376 т. Главньаш потребителями М. р. являются США, Великобритания, Германия, Франция, Бельгия и в последние годы Италия. Главными экспортерами М. р. на мировом рынке являются (данные на 1927 г.): Брит. Индия 857 364 т, СССР 784 686 т. Золотой Берег 450 ООО т, Бразилия 241 823 т, Египет 167 ООО т. В общей сумме 784 686 т экспорта марганцевых руд СССР в 1927 г., как и в предшествовавшие годы, преоб.чадают чиатурские руды- 578 357 т, или 73,7%. Остальные 26,3% падают на никопольские М. р., вывезенные в 1927 г.- за границу в количестве 206 329 т. Главнейшими потребителями экспортных руд СССР являются Германия и США. Потребление М. р. СССР внутри страны, преимущественно никопольских, составляло в 1927 г. 262 460 т. Главными потребителями являются южные металлургич. з-ды. Лит.: Серн А. Ю., Марганец, Обзор минеральных ресурсов СССР, в. 24, Л., 1927 (приложен перечень 195 статей по этому вопросу); его те. Марганец, Годовой обзор минер, ресурсов СССР за 1926-27 гг., стр. 547-575, Л., 1928 (приложен перечень 27 статей по тому же вопросу). А. Жалнговснмй. МАРГАРИН, пищевой жир, представляющий собой стойкую эму.чьсию из животных и растительных жиров с молоком, с добавлением небольших количеств других ингредиентов (поваренной соли, яичных желтков, краски, крахмала), похожий по своему составу, консистенции, цвету, вкусу и запаху на коровье масло. Однако, в то время как в коровьем масле все 100% жира получены из коровьего молока, в М. жир коровьего молока составляет весьма незначительный процент. М. впервые был приготовлен Франц: химиком Меж-Мурье (Mege-Mou-ries) в 1869 г. по заказу французского правительства. На рьгаок вьшускается М. трех типов, соответственно основным типам коровьего масла: сладкого коровьего масла (сливочного), соленого (т.н. экспортного) и топленого. Ббльшая часть М. выпускается в виде соленого продукта-как наиболее стойкого при хранении. М., как и коровье масло, относится к скоропортящимся продуктам. Устойчивость его при хранении примерно такая же, как и коровьего масла. Лучше всего М. сохраняется при t° от -6 до -8°. Сравнительные данные о составе, усвояемости и калорийности М. и коровьего масла (из кислых сливок, просоленного) даны в табл. 1 (по Кенигу). Из таблицы видно, что по составу, усвояемости, теплоте сгорания и коэф-ту использования М..весьма близок к коровьему маслу. \ .-С остав и свойства маргарина и коровьего масла. Маргарин просоленный Коровье масло Общее ко.тичество пищевых щ е с т в (в %)
М. придает пище приятный аромат и вкус; тесто на нем хорошо всходит. Отрицательным качеством М. считают полное отсутствие или незначительное содержание в нем витамина А, присутствующего в коровьем масле. Кроме того М. часто содержит гидрированные жиры (см. Гидрогенизация жиров), вследствие чего возможно присутствие в нем следов никеля, а также так назыв. новых к-т гидрогенизации; последние отрицательно влияют на устойчивость продукта; но в М., содержащем гидрированные жиры, полученные по способу Лёша, эти отрицательные факторы сводятся почти к нулю. Первоначально жировая основа М. составлялась исключительно из животных жиров и гл. обр. из олеомаргарина,-полужидкой части, получаемой из топленого говяжьего сала после отпрессования стеарина (такой М. иногда назьшают маргарином МежМурье). Однако в настоящее время такой состав имеют только лучшие и наиболее до- Табп. 3.-Требо вания, п р е д ъ я в л й в мыв ства марга рогие сорта М.; чаще всего М. вырабатьшают из смеси животных и растительных жиров, а в последнее время-также и из одних раст тительных жиров. По данньш специальной литературы, удельный вес животных жиров в датском М. изменялся следующим образом: 1907 г.-75%, 1923 г.-7,5% и 1925 г.- 5,5%. Вообще же состав жировой смеси для М. весьма различен и находится в зависимости от времени года, от вида и сорта М., отрывочной конъюнктуры на отдельные жирь* и масла. Примерные составы жировой смеси для обычньЕх сортов герм. М. приведены в табл. 2 (по Г. Францену). Т абл. 2.-с о с т а в шировой смеси для маргарина (в %).
Названием первый сок (premier jus> принято обозначать вытопленный при 45- 50° жир говяяшего сала (парного). В последние годы германск. маргариновая промышленность начала с успехом применять подсолнечное масло (экспортное из СССР). В Голландии на М. перерабатывается значительное количество льняного масла в гидрированном виде. В сев, странах на приготовление М. идут гидрированные свежие рыбий жир и ворвань, дающие с молоком хорошие эмульсии; широкое применение для находит кокосовое масло. В СССР маргариновое производство строится на базе растительных масел: подсолнечного, хлопкового,. R тшрАы, допускаемым дяя проязвод-рина в СССР.
соевого как в натуральном, так и в гидрированном виде. Вообще же для приготовления маргарина мог^т служить только жиры и масла, которые разрещены для питания человека; они д. б. совершенно свежие, чистые и свободные от каких-либо примесей. Растительные масла применяются исключительно рафинированные. Согласно постановлению Наркомздрава и ВСНХ РСФСР жиры, предназначенные для М., должны удовлетворять требованиям, изложенным в табл. 3. Одной из главных частей М. является молоко. Оно служит носителем двух важных свойств М.: запаха и вкуса. Молоко, служащее для приготовления М., может быть цельное, снятое и центрифугированное. Оно д. б. обязательно пастеризовано путем нагрева до 65-70° не менее 30 м. (или до 71-75° не менее 20 м. или до 76-80° не менее 3 м.) и последующего быстрого охлаждения до 3-5°. Молоко употребляется чаще всего в виде снятого кислого молока, сквашенного до определенной степени окисленин чистыми культурами молочнокислых бактерий (Bacterium lactis acidi), придающего М. более резкий аромат коровьего масла. Молоко вводится в М. в количестве 15-40% к весу М. На подготовку молока необходимо обращать особое внимание, т. к. от его качества зависит не только запах и вкус, но и стойкость М. В последнее время за границей значительные размеры приняло употребление в М. растворимого в воде сухого молока-порошка (см. Молоко). Для предохранения маргарина от быстрой порчи к нему прибавляют в качестве консервирующего вещества поваренную соль в количестве 2-4%, а ташке бензойную к-ту и ее соли в количестве 0,2- 0,4% (в СССР разрешается добавление исключительно поваренной соли в количестве до 2,5%). Поваренная соль д. б. выварочная и удовлетворять требованиям Общесоюзного стандарта [Ц. Для придания М. желтоватой окраски, делающей его и по цвету похожим на коровье масло, употребляют растворимые в жире расштельные краски-орлеан и куркуму, а в последнее время за границей широкое распространение получили две анилиновые краски-Суданские1и2.В СССР для подкрашивания М. допускаются лишь чистые растительные желтые краски, разрешенные для подкрашивания пищевых продуктов циркуляром Наркомздрава РСФСР (№ 32 от 4/II 1925 г.). Прибавление в М. куриных яичных желтков имеет двоякое значение: способствует образованию прочной эмульсии жиров с молоком и придает М. при поджаривании свойства коровьего масла, т. е. спокойную пенистость и способность давать бурую корку-подрумянивать поджариваемый продукт. Желтки прибавляют непосредственно после вьщеления их из свежих яиц. Обычно желтки (ок. 1% к весу М.) замешивают с молоком и смесь пастеризуют. Употребляются в маргариновом производстве и консервированные поваренной солью желтки, а чаще всего сухой яичный порошок. В последнее время за границей получает распространение гелиоцитин, стойкий и концентрированный препарат, изготовляемый из яичных же.ттков и со- держащий лецитин, холестерин и жир желтков; гелиоцитина требуется значительно меньше, чем желтков. Наряду с яичнылтн желтками и порошком широкое распространение имеет теперь также растительный белок, гл. обр. лецитин в форме препарата витамаргина, обладающего большой эмульгирующей способностью. Получается преимущественно из соевых бобов как побочный продукт при переработке бобов на масло и муку. Прибавление яичных желтков и препаратов из них в М. витаминизирует его, т. к. желтки содержат растворимый в жирах витамин А. Для обнаружения фальсификации маргарином коровьего масла при фабрикации маргарина к нему прибавляют кунжутного или рафинированного хлошсового масла (не менее 5%) или крахмала (0,3%), легко от-крьшаемых при помощи соответствующих цветных реакций. Употребляемый при этодг крахмал не должен содержать каких-либо посторонних примесей и д. б. свободен от микроорганизмов, способных оказывать неблагоириотное действие на качество М. За границей иногда для усиления аромата М, к нему прибавляют летучие кислоты, их альдегиды и глицерин. Обычно для этой цели применяются пропионовая, масляная и капроновая кислоты. В СССР прибавление к М. искусственных ароматических веществ воспрещается. Наркомздравом и ВСНХ РСФС,Р разработаны в- 1928 году (циркуляр Наркомздрава № 98) следующие нормы для маргарина: М. должен при темп-ре 10-15° представлять собою однородную массу плотной пластической консцстенции и давать в разрезе ровную слабо блестящую, слегка влажную поверхность, свободнуто от кристаллов соли; он должен легко намазываться на поверхность, а при жарении пениться, как натуральное коровье масло, и не давать сильного разбрызгивания и треска; цвет М. д. б. бледно-желтый или желтый, равномерный во всей массе продукта; запах и вкус-коровьего масла; содержание ншров < 82%; 1°пл. вытопленного жира не выше 36°; степень кислотности >2,5° Кеттсторфера;содержание поваренной соли > 2,5%;содержание крахмала > 0,3%. Допускается к обращению и топленый М., полученный путем вытопки'жира из готового М. или из полуфабриката; топленый М. должен содержать < 99% жиров и иметь кислотность > 3° Кеттсторфера. Отпуск М. для индивидуального потребления допускается лишь в оригинальной упаковке по 250, 500 и 1 ООО г, для массового потребления-в бочках и ящиках по 10, 50 и 100 кг. В обоих случаях на таре д. б. обозначены: название продукта и жиров, входящих в его состав, название предприятия, а также дата изготовления. Анализ М. производится теми же методами, что и анализ коровьего масла. Прежде всего определяют консистенцию, цвет, запах и вкус продукта, затем его свойства при жарении-разбрызгивание и образование коричневой корки. Если продукт вызывает подозрение, прибегают к микроскопическому исследованию (на плесневые грибки, бактерии и т. д.) и к определению ха- рактера и содержания посторонних и недозволенных веществ (парафина, искусственных ароматических веществ, анилиновых красок, консервирующих веществ). Далее определяют содержание жира, воды, казеина, молочного сахара, молочной кислоты, поваренной соли, крахмала. В выгопленном и осветленном жир^ определяют: точку плавления, точку заст1лвания, удельный вес при 100°, показание бутирорефрактометра при 40°, кислотное число, йодное число, число омыления, число Рейхерт-Мейсля, число По-ленске, число Генера. Присутствие животных жиров открывают при помощи характерных свойств заключающегося в них холестерина. Гидрированные жиры распознают путем реакции на присутствующую в них изоолеиновую к-ту. Яичный желток откры- Жир 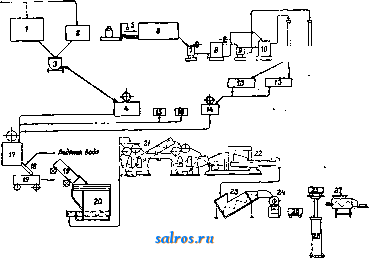 Фаг. I. вают по способу Фендяера обработкой М. раствором поваренной соли и дальнейшей обработкой фильтрата дымящей соляной к-той [*]. Лецш-ин определяют по содержанию в продукте фосфора. .Общая схема современного производства М^ представлена на фиг. 1. Рафинированные жидкие масла поступают в баки-приемники 1, твердые жиры (гидрированные), олеомаргарин, первый сок, смалец (все в растопленном виде)-в баки 2, при этом для каждого вида масла и жира имеется особый приемник. Из каждого приемника нужное для составления жиро-* I вой смеси количество жира спускается в бак подвижных весов 5, катящихся по рельсовому пути, откуда вся жировая н а-садка передается в темперировоч-ный котел 4 (отдельно изображен на фиг. 2)-двустенный цилиндрич. котел с мешалкою и заложенными между его двойными стенками паровым и водяным змеевиками. В темперировочном котле жировая смесь выдерживается при постоянном поме-  Фяг. 2. шивании при t° от 28 до 32**. Одновременно с подготовкой жировой смеси ведется подготовка молока. Молоко (цельное) из бидонов 5 сливается в развесочный бак, установленный на подвижных весах, и через фильтр попадает в приемник 6, откуда поступает в непрерывно действуюпщй подогреватель 7, в котором нагревается до 1° 45°. Далее молоко проходит через непрерывно действующий сепаратор 8, в котором разделяется на сливки и снятое молоко. Сливки, пройдя через пастеризатор 9, трубчатый холодильник и будучи далее подвергнуты закваске и вызреванию, поступают в маслосбиватель 11, в котором и сбиваются на масло. Снятое молоко совершает следующий путь: пастеризатор 10, водяной поверхностный холодильник 12 (охлаждает-оя до 15°), ванны для молочнокислого брожения 13 и темперировочный котел 14; в последнем сквашенное молоко доводится то-g асйосбаыт 6 ДО t° 28-32°. Вся аппаратура для переработки молока должна быть луженая. В бачках 15 и 16 приготовляется краска и яичные желтки. Краску замешивают с растительным маслом, яичные желтки добавляют замешенными со сквашенным молоком. Жировая смесь и сквашенное молоко из темперировочн. котлов 4 и 14, а также краска и желтки поступают в к и р н-м а ш и н у 17 (она отдельно изображена на фит. 3)-луженый двустенный бак овальной формы вместимостью от 0,5 до 3 т, с заложенными между стенками змеевиками для воды и пара, и снабженный быстро вращающейся лопастной мешалкой. Наблюдения за процессом в кирн-машине производятся через смотровое окошко и по термсааетру: по мере образования эмульсии нрозрачва^Ез всплески смеси мутнеют и под конец совершенно теряют прозрачность; t° постепенно падает, затем внезапно останавливается и даже поднимается на несколько градусов-зто момент наиболее интенсивного образования и схватывания (за-стьшания) эмульсии. Когда же температура начинает снова падать, процесс эмульсирования считается за-конченньш, убавляют скорость вращения мешалки и приступают к выпуску готовой эмульсии из кирн-машины. Весь процесс эмульсирования в кирн-машине длится ок. 30 минут. Следующая операция-быстрое заморажргеание выпускаемой из кирн-машины эмульсии, которое может производиться двумя способами: мокрым и сухим.  Фиг. 3. 1 ... 24 25 26 27 28 29 30 ... 48 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
© 2007 SALROS.RU
ПромСтройМат |