 |
 |
 |
 |
1 ... 23 24 25 26 27 28 29 ... 48 та-воронви. Т. к, сжатый воздух при выходе из сопла охлаждается, а нормальная окраска требует i° не ниже 20-25, аппараты чзнабжают подохревате^ем (электрическим, паровым или,газовым). Давление воздуха, в зависимости от размера отверстия распылителя и от плотности красочного состава, колеблется от 0,2 до 3,5 atm (избыточного давления). Для тщательной окраски требуется давление от 2,5 до 3 atm, при диаметре отверстия сопла в 2 мм. Т. к. при работе с краскораспылителями образуется тухман, содержащий частицы красок, вредный для здоровья маляра-краскодува, то применяют соответствующие приспособления, улавливающие и собирающие мелкие частицы красочного состава и снабженные очистительными фильтрами, трубопроводом для удаления вредных газов и испарений. В настоящее время механизация строительно-малярных работ в СССР, постепенно и планомерно вытесняет ручную работу кистью. Для малярных работ на трансцорте применяют сложные агрегаты в ааде передаиящых компрес-г сорных установок, специальных автоматич. окрашивателей в один и в два цвета, а также для окраски деталей со всех сторон, внутренних поверхностей труб, для лакировки мелких массовых изделий и т. п. Для окраски или лакировки вагонов существуют специальные кабины. Малярные работы, по существу являющиеся технологич. процессами, связаны с нзобразите.тьными искусствами, в особенно--сти в отрасли монументальной живописи: до последнего времени красочная обработка поверхности помещений носила характер отчасти прикладной, отчасти орнаментный, решительное упрощение современной архитектуры-отказ от какой бы то Ш1 было декоративности, от украшенчества -заставляет особенно серьезно углубить проблему цветового оформления сооружений, а благодаря разработке и практич. использованию теории проф. Оствальда (готовые нормированные колера) задача красочного офор-лщгевия строительных или вшбщ© .Щ)оз№Ш-ленных объектов значительно облегчается. Лит.: Оссовеф[иий: И., Малярное дело, 2 изд., Петербург, 1897; Приоров М., Малярное дело, -стекольные работы и 01 лейка обоями, Москва, 1896; Э и г е л ь Ф., Малярные работы, пер. с немецкого, <:;ПБ, 1904; г и л л и X Г., Современный маляр, СПВ, 191>9; Термин Р., Живописец-маляр, 2. издание, -СПБ, 1899; Семенов А., Малярные краски, 2 изд., М., 1925; Григорьев Н., Малярное дело, 2 изд., М.-Л., 1927; Зелен ков В. А., Малярное дело, -Л,- М., 1928; Антокольский Л., Программа кружков но и.чучению малярных работ, Москва, 1928; Киселе в В, С, Олифа и лаки, М.-Л., 1926; его ж е. Краски, масла и лаки, М.-Д., 1926; Временный справочник цлп составления производств, смет на малярные работы, -2 изд., М., 1927; Песоцкие И. и А., Малярное дело, 2 издание, М.-Д., 1928; Трубецкой В. А., Механизация малярных работ на транспорте. М., 1929; Михайлов С П., Произ-зодство минеральных и вемляных красок. П., 1915; Н 1 И 1 g Н., OruDdzuge d. Mai- u. Anstrlchtechnlk, В., 1924; Andes L., Prakt. Handbuch fur Anstreicher 11. Larklrer, 5 Aufl., W.-Lpz., 1922; P h 1 e p s H., Das ABC d. farbigen Aussenarcbitektur, Fachausschu.s8 fur Anstrichtpclmik beim Verein deutscher Тп{?еа1еиге , H. 1-Vergleicbende Versuche mjt Farbspritzplstolen, В., 1929; Vortrusre, eehalt. auf d. Jahresversammlun 1929 zu Wien, Veranst. vom Reichsausschuss fiir Metall-scbutz, e. v., Berlin u. d. Oesterr., Ausscbuss fiir Metall-schutz, Wien-Berlin, 1929; Bersch J., Fabrlkation d. Mineral- und Lckfarben, 2 Auflage, W.-Lpz., 4893; J e n n 1 8 о n Fr., Herstellun? v. Parblacken us kunstllcben Farbstoffen, Dresden, 1901; M I e r- a г i n s к 1 St., Erd-, Mineral- u. Laakfarben, Шге Darstellung, Priifung und Anwendung, B, 1-, Wien- Lpz., 1898; Le petit manuel du peintre en butiment, P., 1924. Л. Антональсняй m C. Михайлов. ПрофвеоиФиадьные вредности. В отношении характера профессиональных вредностей малярных работ необходимо отличать ручную окраску от механической (пневматической). При ручной окраске главное значение имеют характер и состав краски; при пневматич. окраске главным определяющим вредность фактором являются растворители и разжижители краски. При малярной обработке предметов, уже подвергшихся окраске, возникают вредности, обусловленные работами по очистке старой краски. Применявшееся раньше весьма широко сухое соскабливание. краски в последнее время встречается все реже. До настоящего времени сохранился способ сжигания краски (паяльная лампа, жаровни, установки для автогенной резки и др.), при котором, особенно при счистке красок, содержащих свинец, образуется так называемый воздушный свинцовый коллоид , вызывающий отравления уж;е при малых вонцеитрацнях его в воздухе. В последнее время для влажного удаления старой краски все большее распространение получают различные жидкости и мастики. Многие из них содержат вещества(бензол, каустич. сода и др.), делающие их вредными в смысле ожогов. Произведенное Центральной испытательной лабораторией ЦНИУ НКПС совместно с Государственным научным институтом охраны труда^ испьггание различных мастик, применявшихся для счистки старой краски с железной обшивки ж.-д. вагонов, показало, что технически удовлетворительной, а также экономичной и относительно безвредной является мастика следующего состава (в весовых %): 35% негашеной извести, 7% кальцинированной соды, 7% мела и 51% воды. Из всех процессов работы при ручной окраске найболывее профессионально-гигие-вжч. значшие имеют моменты, связанные с образованием пыли и загрязнением ею воздуха рабочих помещений. К этим процессам относятся работы по смешению сухих красок с олифой или другими веществами, фальцовка или счистка подготовляемой для окраски поверхности, а также все промежуточные стадии окраски, заключающиеся в выравнивании и сглаживании неровностей и шероховатостей на нижних слоях красок перед наложением на них последующих слоев. Особенно вредными и угрожающими здоровью рабочих являются (по характеру и степени вредности, а также в силу своей чрезвычайной распространенности) свинцовые краски, в особенности свинцовые белила. Профессиональные заболевания, вызываемые свинцом, относятся к самым тяжелым заболеваниям этого рода. Непосредственной причиной их возникновения в большинстве случаев является вдыхание свинцовой пыли, к-рая при дальнейшем прохождении через дыхательные пути в легкие вызывает различные заболевания этих органов или попадает.в организм через желудочно-кишечны!! тракт; основная задача по борьбе с вредностью этих красок заключается в полном устранении возможности проника- *! &бя. 1.-С о с та в НИЯ яда В организм, что по существу достижимо толькр при замене свинцовых красок другими безвредными красителями. Заменяющими свинцовые белила красками, вполне оправдавшими себя с технич. стороны и не встречающими возражений с гигиенич. точки зрения, в настоящее время признаны для наружных окрасок титановые и цинковые белила, а для внутренних-кроме того и литопон. При механической окраске основные вредности обусловливаются применением быстро сохнущих красок и лаков (цапоновых, ни-троцеллюлозных и др.), приготовляемых на ядовитых растворителях (бензине, бенэоле,-амилацетате, метиловом спирте, ацетоне и др.). Характер работы при пневматической окраске вызывает образование облаков крабок и лаков, попадаюнщх в воздух в капельножидком состоянии, испарение же этих растворителей вызывает образование газообразных ядовитых веществ. Вдыхание их при известных концентрациях их в воздухе может вызвать тяжелые отравления. Борьба с последними вначительно облегчается применением соотввгствуюпшх вежшлшщонных установок, а также путем, замены ядовитых растворителей менее токсичшлш. В СССР Наркомтрудом издано несколько обязательных постановлений, направленных к ограничению выработки и применения свинцовых белил. Постановление, изданное в 1929 году, запрещает упоор^Йление свинцовых белил в маллфном деле за исключением весьма ограниченной группы работ (при окраске судов, мостов и др.), где употребление свинцовых белил разрешено временно до 1 января 1935 года. Запрещение применения свинцовых красок не ка-саетбя тгбка дргт свинцовых Соединений (сурика, крона и др.). Наркомтруд издал обязательное постановление по охране труда лиц, занятых работами по пневматич. окраске. Постановление это предусматривает обязательное устройство вентиляционных установок при всех работах, где это воз-м<шво по техническ. условиям; кроме того запрещается приме-ншие свинцовых красок и применение бензола в качестве растворителя лаков, а также предписывается обязательность устройства на предприятиях ряда са-нитарно-технических установок, которые давали бы возможность рабочим соблюдать правила личной гигиены (мытье, еда в специально отведенном помещении и т. п.), и наконец предписывается обязательное применение рабочими индивидуальных защитных приспособлений (спецодежда, респираторы, очки, рукавицы и т. п.). Лит.: в в е д е н к и н С. Г., Об удалении старой краски с металлич. обшивки пассаж, вагонов мокрым путем, Москва, 1930; Дмитриев М. М., К оздоровлению условий труда маляров, Труды Ленингр. института гигиены труда и техники безопасности , М., 1930, т. 3, вып. 4; Map г один Л. И., Свин- цовое отравление у автогенные резчиков бтарйх судо и борьба с ним, там же; La cijuse, Geneve, 1927, В8Д< Международного бюро труда; W е п z е 1-А 1 v е п 1 е b е n-W 111, Die Bcseitigung der beim Tauch-u; Spritzlackieren entstehenden Dumpfe, Schriften au d. Gesamtgebiet d. Gewerbebyglene, brsg. v. d Deutscb* GMellschaft fiir Gewerbehygiene In Frankfurt a/M., H. 48. в., 1997. Д. Наган. МАЛЯРНЫЕ КРАСКИ, см. Малярное дело. М А Н Г А Н И Н, медно - марганцево - никеле-сплав красноватого цвета, высокого электрич. сопротивления, применяемый гл. обр. для эталонов постоянного сопротивления, в меньшей степени для буферных сопротивлений и отчасти для термопар и нагревательных приборов. Присадка Мп к Сп обусловливает снижение теплового коэф-та сопротивления, а присадка Ni-снижение термоэлектродвижущей силы в отношении Си. Настоящий М., предложенный в 1889 г., состоит из 84% Си, 12% Мп и 4% Ni; однако-к группе М. относят разные другие сплавы, в которых Мп содернштся больше, чем Ni (напр. т а р н ак)и кроме того родственные по свойствам сплавы, в к-рых Ni заменен Ке(ферроманганин, рвзистин> или А1 (с п л а в Терло), причем содержание аретьего компонента меньше, чем со-держаете марганца. Сокга-в сплавов, удерживающих сшиое штвшт М. взт родствек--ных ему по свойствам, предсташхен в табя. 1. манганинов я родственных сплаве в (в %).
М. характеризуется значительным удельным электросопротивлением (хотя и меньшим чем у константана), малым 4°-ным коэф-том электросопротивления (около 2-10 , а в известных случаях 3-10 * и даже до 1-10~ ); при известных соотношениях компонентов-тепловой коэф-т сопротивления подобных сплавов Сп-Мп может оказаться, как впервые открыто Вестоном, отрицательным []. Сопротивление настоящего М. меняется с t не лршейно, и ок. 30° скорость изменения максимальна. Нек-рые сравнительные данные относительно электросопротивления М. и других сплавов высокого сопротивления сопоставлены в табл. 2. Термоэлектродви жущая сила лданганиново-мщной пары со- МАНГАНИН 51& Таб-л,- а.- Данные о с о я р о т и в л е н и и некоторых сплавов.
ставляет 3-4 fiV/°C, тогда как у константа-ново-медной пары термо-эдс составляет 40 piV/°C. Температура твшшт М. <шка (см. Cnp.TBt т. II, Дтврамт рвштст} так что расплавляющий ток шателен; в табл. 3 сопоставлены данные относительно Табл. 3.--С яла расплавляющего тона в зависимости от диаметра проволок и (длина в 100 мм) в А.
зависимости между диаметром проволоки и расплавляющим ее током для М. и нек-рых сплавов; из нее видно, что М. превосходит все сплавы за исключением платино-ириди-евого. Физические константы М.: уд. в. 8,4, уд. теплоемкость 0,097. Электросопротивление манганина наиболее устойчиво в отношении 1° при содержании 12% Мп; малая изменяемость сопротивления от времени м. б. достигнута нагревом М. до 700° в течение нескольких мин. в атмосфере углекислоты, а затем прогревом при 150° в течение 4-5 ч. в масле; удовлетворительная термическая обработка м. б. произведена нагреванием до 140°, но лишь после покрытия М. шеллаком; в противном случае на поверхности М. образуется медная пленка, к-рая д. б. счищена. Подобные меры предосторожности необходимы в виду легкой окисляемости М., особенно при нагреве, вследствие чего предел рабочей t° для М., как и для сплава Терло, только 100°. Однако необходимо иметь в виду, что сопротивление и термически обработанного М. с течением времени растет примерно на 0,07 % в год (а в нек-рых случаях менее, чем на 0,001 %). Из числа различных Cu-Mn-Ni-сплавов М. особенно пригоден для эталонных сопротивлений; остальные аналогичные сплавы, об- ладая меньшим тепловым коэфидиентом сопротивления, частью превосходят манганин по термо-эдс, частью уступают ему. После многолетних испытаний в Reichsantalt было установлено, что М., принятый в Германии для эталонных сопротивлений, во всяком случав более пригоден, чем платиново-се-ребряный сплав, нормализованный в свое время для той же цели в Великобритании и во Франции. Однако замена никеля более дешевыми железом (ферроманганины, ре-зистиньх) или алюминием (сплав Терло и др.) понижает <°-ный коэф-т сопротивления и термо-эдс в отношении меди; так например, у ферроманганина, указанного в табл. 1, термо-эдс в отношении меди равна нулю, а у сплава ТерлО она составляет 0,3 fxV/°C. Температурный коэф-т сопротивления у этих сплавов изменяется в зависимости от состава и термической обработки и м. б. как положи-теяк^ш, так и отрицательным. Настоящий М. поступает на рынок в вид© проволоки (прутьев) диам. 12 мм и листов толщиною от 0,2 лш, шириною 60 лш. Протрава продажного товара бывает как красная, так и белая, однако в последнем случае при паянии серебром листы краснеют, и тогда требуется вторичная протрава после паяния. Сплав Терло характеризуется кроме вышеприведенных еще и следующими данными: удельный вес 8,15; сопротивление на разрыв 55 кг/мм; коэфициент линейного расширения 0,0000194. Конструкция германских сопротивлений разработана К. Фюсснером. Манганиновые сопротивления изготовляют в пределах от 0,0001 до 100 000 Q, причем на сопротивления меньшие 0,1 а идет листовой М.,а на ббльшие 0,1 й-манганиновая проволока, обвитая шелком; эта проволока наматывается бифилярно на изолированную шелковой лентой латунную трубку, затем обмотку продйтывают шеллаком и подвергают дли- тельному остариванию приблизительно при температуре 120°. После этого ее вставляют в латунный футляр (гильзу), в которую вводятся через эбонитовую крышку толстые медные токоприводы. Для устойчивости сопротивлений необходимо защищать обмотку от колебаний атмосферной влажности, так как при ее изменении шеллак изменяет натяжение проволоки и следовательно ее сопротивление. Эта неустойчивость устраняется герметической закупоркой гильз или содержанием обмоток в атмосфере постоянной влажности. Резистин кроме указанного для манганина электротехнич. применения идет также в машиностроении на двигатели внутреннего сгорания, паровые турбины и паровые машины. Производство М. и подобных ему сплавов представляет известные трудности и стоит дорого, т. к. материалы должны-отличаться большою чистотою; в частности требуется вполне удалить из сплава попадающий туда вместе с Fe и Мп углерод, к-рый сильно понийсает сопротивление готового материала. Поэтому для получения М. обычно исходят из хлористых солей Ре и^ Mn, смесь к-рых в растворе обрабатывают известью: FeCU+MnCl,-l-2Ca(OH)a=Fe(OH),+Mn(OH)j+2CaClg. Осадок гидратов Fe и Мп промывают, высушивают и восстанавливают углем при высокой Г. Далее полученный т. о. ферромарганец сплавляют с чистой рафинированной медью [*,]. Плавка ведется либо в магнезиальных тиглях либо в графитовых с облицовкой из MgO; тигли из глины или алунда для данной цели непригодны, т. к. вводят в сплав кремний. Работа ведется в электрич. печах сопротивления и притом в токе углекислоты. Лит.: 1) Ам. П. 381 30Г. П. 95443; 8)S р ег-гу Е. S., oJahresberlchten fur chem. Techa.*, Lpz., 1906, p. 288; Жемчужный C. и Уразов Г., ЖРХО , 1907, т. 39, стр. 787 (сплавы Мп с Си и Ni); Ж е м ч у нс п ы й С. иНемилов В., Известия Института физико-химич. анализа . Л., 1924, т. 2, стр. 450 (Исследовааие электрич. сопротивления и t°-aoro коэф-та сплавов манганинового ряда); Ш е м-чу5кяыйс. и Погодин С, там же, стр, 464 <0 (°-ном коэф-те электрич. сопротивления манганина и константана); Жемчужный С- я Погодин С, Сплавы для электрич. измерительных и нагрева-тельныхпрНоров, Л- 1928; J а е g е г W., ElektrlscUe MessteChuikfS Aull., Lpz., 1928; F И й s n e г K.u. L i н-dek St., Zt$obr. f. laetmmeiifenltttride*, B. 188Э; B.9,p. 23.3J t8 5B. ib,[Ui §94; FiissweijJE, evbta d e к St., Wis8en8chaftUche АмадГ sikalisch-technischen Reicbsanstait*. В., 1895; p. SO I, F u 8 8 n e r K., eVerbandlungea der physlkaltscliert Gesellschaft*, 1891, B. 10, p. 103; FQasner K., ETZ> , 1892, B. 1 3, p. 99; L i n d e к St., Repoct of the British Association for the Advancement of Sciences, L., 1ЙУ2; Jaeger W. u. L i n d e к St., eZtsohr. t. Iastiumentenkunde , В., 1898, В. 18, p. 97; 1906, В. 26, p. 15; J aege r W. u. L i n d e к St., Wledc-manns Annalen , Lpz., 1 898, B. 65, p 572: Jaeger W. u. S t e n w e h r H. v., eZtschr. fur lastrumenten-kunde , Berlin, 1913, B. 33, p. 293; S t en w e h r. H. u. S с h u l.z e. A., WissenschaftlIche Abhandlungen der physikalisch-technischen Reichsanstall*, Berlin, 1927,p.75; S p e г ry E. S., Brase.World ,N.Y.,190j, p. 255; В ash F. E., Chemi8Ches Zentralblatt*, В., i920, sechste Folge, Jahrg. 2, p. 289; Jabresberlcht9 f. chem. Technik*, 1890, p. 432. П. Фпорвнекий. МАНИЛЬСКАЯ ПЕНЬКА, см. Банановое еолошю. Волокна прядильные. МАННЕСМАНА СПОСОБ ПРОКАТКИ ТРУБ, СМ. Трубы. МАНЯИТ, d-маннйт, СвНвСОШа, шестизначный спирт; большие количества манни-та содерз1ш,тея в соке различных южных и тропических рас-тевгий-наприм. ясеня, Fraxinus ornus (Сицилия) и Myoporum pla-ticarpum (Австралия). Получают М. из так наз. манн ы-высушенного сока растения, в к-ром содержится 55-90% маннита и ШОН откуда его извлекают горячей водой; синтетически М. получается восстановлением d-маннозы и d-фруктозн. М. кристаллизуется в ромбйч. призмах; <° л. 165- 166°; уд. в. 1,52; уд. вращение [а]о=- 0,25°; растворим в холодной воде, очень мало в спирте и совсем нерастворим в эфире. При окислении азотной к-той дает смесь d-маннозы и d-фруктозы, при биологич. окислении бактериями (В. xylinum)-d-фруктозу. Применяется М. для приготовления таблеток, служащих заменой сахара для диабетиков. Для той же цели служит дульцино л- препарат, приготовляемый из М. прибавлением к нему поваренной соли. п. шорыгчн. Лит.: см. Углеводы. МАННОЗА, CeHiaOe, углевод, принадле-.жащий к моносахаридам. Наиболее извест- СНаОН сн Ь.н и с. он H-ioH но с-н нс-он н ный стереоизомер, d-манноза, сра]1тельно редко встречается в растениях в свободном состоянии (например в апельсинной корке, в (но)сн Amorphophallus Konjak и др.) или в виде глюкозидов (нап]()и-мер в строфантине); гораздо ча-,)ще-в виде высших углеводов, т. н. м а н н ан о в, к-рые дают при гидролизе или одну М. или смесь ее с другими моносахаридами. Маннаны являьотся ре-н2(0Н) зервным веществом рвзличных пальм, содержатся в скорлупе каменного орезш., в цареградских стручках, в зернах ячменя и пшеницы, в дрожжах ит. д. Получают маннозу кипячением скорлупы каменного ореха (отбросов пуговичного производства) с разбавленной соляной к-той. Впервые М. была получена Э. Фишером (1888 г.) синте-тич. путем-окислением природного d-ман-нита (см. Манпит) азотцо к-той. М. кристаллизуется из спирта в ромбич. призмах сладкого вкуса; 132°; очень легко растворима в воде (248 ч. М. в, 100 ч. воды при 17°), трудно-в спирте. В растворе показывает мутаротацию с изменением на-йшшгеетя вращения от -16,5° до Н-14,2°. расположение аСимметри<1Ных атомов углерода, бдижайших к альдегидной группе); это явствует из их взаимных превращений при действии слабых щелочей, из идентичности фенилозазонов обоих моносахарвдов и т. д. При восстановлении М. с^разувтся d-маннит, при окислении-одноосновная d-манноновая к-та, СН2(ОН)-(СНОН)4-СООН, затем дву основная d-манносахарная кислота, СООН (СН0Н)4 СООН. М. сбраживается дрожй^ми подобно d-глюкозе. п. шорыгаи. Лит.: см. Углеводы. МА110ДЕТАЙДЕР, р е д у к т о р, прибор для понингения давления при истечении газа из одного сосуда в другой. В проьшш-ленной практике М. применяют для понижения давления газов со 150 до 10-0,2 atm. При Зтой газ заключен в баллщда) (см.).Наи-бййЕЫйШ йрй1ш^ве1вш Ш, вшёг Iff деле--дйй поншййя ДавЙш. кислорода и ацетилена в баллонах до рабочего давления в горелке. М. для кислорода и ацетилена отличаются друг от друга как породу металла, из которого они изготовлены, так и по конструкции. Основной материал М. для кислорода- латунь, для ацетилена - железо, сталь. Чугунную отливку для изготовлеция М. обоих типов применять воспреадейо. 11. для кислорода имеет применение и для редуцирования других газов (сжатого воздуха, углекислоты, водорода и т. д.), при условии отсутствия химич. влияния газа на медные сплавы. М. окрашивают для кислорода в синий, для водорода в красный, для ацетилена в белый цвет. М. для кислорода прикрепляется к вентилю баллона при помопщ колпачков ой гайки; М. для ацетилена и др. газов под давлением до 15 atm прикрепляется при помощи специальной скобЬт. На фиг. приведена схема М. Камера А при помощи трубки 1 соединена с баллонами. При открытии бутылочного вентиля газ переходит к соплу 2 п в манометр 3. Силой прУ- МАНОМЕТР жины 4 рычаг 5 действует на колпак 12 из твердой резины и закрывает сопло -3.Вращая винт 6, с помощью рычагов 7 и 5 открывают отверстие сопла 2, и газ попадает в камеру А к в манометр 8. Из камеры А через вентиль 9 газ проходит наружу; 10-предохранительный клапан. Сохранение постоянного низкого давления в камере А основано на принципе равновесия сил: давле-L J ния газов, действую- щих на клапан у сопла 5 и на резиновую мембрану 11. Диаметр (в свету) сопла 2 манодетандера к одиноч-HbjM баллонам стандартной емкости равен 2,5 мм, а к группе баллонов-ок. 7,5 мм. Разрез кислородного М. см. Автогенная сварка, фиг. 3. Е. кузмах. Лит.: GM. Ашогенная сварка, МАНОМЕТР, прибор для измерения степени упругости жидкостей и хвзов, заключенных в замкнутом пространстве. В технике М. для измерения упругости меньше одной атмосферы получили специальное название вакууметров (см. Вакуум). (По устройству М. можно разделить на две категории: М. с жидкостью, измеряющие давление высотой столба жидкости, и М. пружинные, измеряющие давление посредством трубчатой пружины или упругой мембраны, изменяющих свою кривизну пропорционально-производимому на их стенки давлению. В лабораторной практике наибольшее применение имеют М. с жидкостью (ртуть, вода, масло и т. п.) вследствие простоты устройства таких приборов, надежности и точности их показаний. В промышленной практике такого рода приборы могут иметь лишь ограниченное применение, так как они неудобны для измерения высоких давлений- и требуют специальной покойной установки и весьма бережного обращения. Для измерения давления в 1 atm ртутный М. должен иметь высоту не менее 0,8 л*, а следовательно для измерения давления напр. 100 atm потребовалась бы длина около 80 м. Если ртуть заменить водой, жидкостью почти в 13,5 раз более легкой, чем ртуть, то для измерения того же давления в 100 atm понадобилась бы трубка длиной почти в 1 км. Самый длинный ртутный М. во всем мире устроен на Эйфелевой башне в Париже; при помощи этого М. можно измерять давления до 400 atm. Для уменьшения высоты М.с жидкостью можно устраивать их в форме ряда U-образных трубок, соединенных меясду собой и наполненных наполовину ртутью, наполовину водой. Общая высота столба жидкости т. о. может быть сделана как угодно большой в зависимости от высоты каждого колена и их числа. В Главной паяате мер и весов в Ленинграде устроен такой М., занимающий относительно небольшое место и дающий возможность измерять с большой точностью давления до 100 atm. При измерении давления ртутным М. необходимо принимать во вш-ь т. э. т. XII.  го >ю so 80 tore Фиг, 1. мание изменение уд. веса ртути с t°; обычно градуировка делается полагая t° столба равной 0°; при более высокой (° необходимо уменьшать показания М. на величину, указанную на графике фиг. 1. Устройство ртутного манометра для измерения небольших 1 давлений или разре- I v жений видно на фиг. 2. Д..- М. пружинные, как выше замечено, основаны на применении металлич. пружины или упругой металлич. мембраны, деформирующихся под действием давления на них жидкости или газа. Если эту деформацию при помощи системы передаточных рьшагов и зубчаток передать вращающейся указательной стрелке, то получится простой прибор для измереш1я давления в том замкнутом пространстве, с к-рым соединена пружина М. Главной частью пружинного М. является дугообразно изогнутая трубка о (фиг. 3) из достаточно упругого материала, имеющая овальное сечение. Если открытый конец этой трубки закрепить неподвижно на стойке б и нагнетать через него в закрытую с другого конца трубку газ или жидкость, то трубка под влиянием внутреннего давления раскручивается и закрытый свободный ее конец отклоняется на угол, пропорциональный, в определенных пределах давлений, величине последнего. Это перемещение конца трубки передается при помсйци тяги в зубчатому сенатору 8, к-рый зацепляется с шестеренкой, сидящей на оси стрелки. Как длина тяги в, так и точка присоединения ее к сектору сделаны изменяющимися, чтобы дать возможность вьшерки прибора, а именно: изменяя длину тяги б, можно поставить стрелку на нуль, а перемещая точку соединения ее с  Фиг. 2.  сектором, изменяют передаточное отношение и таким образом приноравливают его к индивидуальным особенностям пружины. В пластинчатых, или мембранных, М. (фиг. 4) давление измеряется величиной деформации упругой мембраны а; движения ее 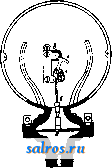 Фиг. 4. передаются стержнем б через промежуточный рычажок в на зубчатый сектор г, зацепляющийся с шестеренкой, которая сидит на оси стрелки. Небольшая спиральная пружина д (фиг. 3 и 4) служит для силового замыкания всех отдельных членов передаточного механизма и предотвращения мертвого хода. Теория манометрической трубки до настоящего времени не может считаться достаточно полно разработанной, и все расчеты, производимые по формулам, предложенным разньпди исследователями этого вопроса, не дают результатов, вполне совпадающих с данными практики. Наиболее удовлетворительное решение этой задачи предложено известным голландским математиком и физиком Лоренцом, который вывел формулу для приб-линсенного расчета размеров манометрической трубки, предназначенной для измерения давлений в определенных пределах. Эта формула вполне подтверждает вьфаботанные Хфакти-кой требования, предъявляемые кманометрич. трубке, а именно: сечение трубки должно иметь овальную форму, причем ббльшая ось овала должна быть перпендикулярна к плоскости витка пружины. При таком устройстве трубка при возрастании внутри ее давления подвергается раскручиванию. Если же малая ось овала перпендикулярна к плоскости витка, то такая трубка с возрастанием давления закручивается. При просвете трубки круговой формы давление не изменяет кривизны трубки, и такая трубка для изготовления манометров не пригодна. В СССР приказом по ВСНХ от 28 февраля 1925 г. № 512 введена обязательная поверка М., устанавливаемых на паровых котлах и других машинах, где требуется измерять давление или разрежение. Поверка М. осуществляется путем присоединения их к замкнутому пространству, в котором поддерживается определенное давление. Величина давления или определяется особо точными, т. п. контрольными М. или обусловливается самым способом образования давления, как напр. в так наз. поршневом М., изображенном на фиг. 5. Поршень а проходит через плотно пришлифованный сальник в цилиндр б, сообщающийся посредством канала в с испытуемыми приборами. В верхней своей части поршень несет платформу, на которую кладут грузы г, рассчитанные таким образом, что каждый из них вызьтает увеличение давления на определенное число единиц. Для этого их делают обычно веса (в кг), кратного эффективной площади поршня в см;  Фиг. 5. последняя несколько отлична от геометрической площади поперечн. сечения поршня и определяется опьггом. Для уничтожения влияния трения между стенками цилшвд-ра и поршнем, последний перед отсчетом приводят во вращение. В виду того-что манометрическая трубка работает правильно только в определенных пределах давлений, как общее правило установлено, что ка-ясдый М. может применяться для измерения давлений, находящихся в пределах между^ i/g и наибольшего давления, для к-рого предназначен данный прибор. Для измерения давления газов или жидкостей, химически действующих на пружину М., применяются трубки из материала, не подвергающегося этому действию. Особенную опасность представляют случаи, когда газ или жидкость могут образовьтать горючее или взрьшчатое соединение с металлом трубки. Поэтому напр. для измерения давления сжатого кислорода нельзя применять М., если в нем имеются какие-либо органич. вещества (масло, бумага и т. п.). Для измерения давления ацетилена нельзя применять М. с медной пружиной,так как образующееся при действии ацетилена соединение с медью- вещество взрывчатое. Для измерения давления аммиака нельзя также применять медные пружины, так как аммиак действует химически на медь и быстро разрушает прибор. Лит.: Сидоров И. И., Манометры, их устройство и поверка, Л., 1928; Мещерский И. В., Временник Главной палаты мер и весов . Л., 1925, вып. 1/13, стр. 120; Gramberg А., Technlscbe Messungen bei Maschlnenuntersuchungen und zur Be-triebskontroUe, 5 Aufl., B. 1, Berlin, 1923; Manometer d. phys.-tecbn. Reichsanstalt, Z. d. VDIi>, 1900, p. 261; Klein, Der Genauigkeitsgrad v. Hochdruck-messern.ibid., 1910, p. 792; Strom e ye r. Remarks on Pressure Gauges, Engineering)>, London, 1907, p. 316; Jacobus, Measuring of Pressures of 10 000 lbs. p. sq. inch, Engineering News , L., 1897, p. 327; Martens, Apparate zur Messung hoher Flfjssigkeits-drucke, Z. d. VDI , 1909, p. 747. A. Доброхотов. МАНОМЕТРИЧЕСКОЕ ПЛАМЯ, пламя газовой горелки, к-рое под влиянием звуковых волн изменяет свою высоту и применяется для исследования частоты звуковых колебаний и приближенного определения формы звуковой кривой. М. п. впервые было применено Р. Кенигом (1862 г.). На фиг. показана капсула для исследования звука при помощи М. п.: светиль- =3 ный газ проходит через кран Ь в камеру а и зажигается у отверстия с. Камера о с одной стороны закрыта тонкой резиновой мембраной АВ, на которую действуют исследуемые звуковые волны. Под влиянием переменного давления в звуковых волнах мембрана АВ создает такое же переменное давление в камере, заполненной газом; вследствие этого пламя с ритмически укорачивается и удлиняется. Периодические изменения длины пламени рассматриваются непосредственно во вращающемся зеркале или фотографируется их отражение в нем; последнее представ.чяет собою или ряд правильных светлых полос (в случае чистого тона) или светлую полосу с различной длины язьпсами. соответствующую форме кривой сложного звука. Марбе  (1906 г.) регистрировал колебания пламени не фотографически, а протягивая над пламенем полоску бумаги, на к-рой оставался след копоти с периодическими потемнениями и посветлениями. Старинный способ ис-. следования звука, М. п. теперь имеет только демонстрационное значение. п. Беликов. МАРГАНЕЦ, Мп, химический элемент VII группы периодич. системы, аналог недавно открытых элементов-мазурия и рения; ат. вес 54,93 (установлен пока один изотоп с ат. массой 55); порядковый номер 25. М.-металл сероватого цвета с красноватым от-тбнком, очень хрупкий; твердость непостоянная, по минералогич. шкале Моса равняется 6 (цифра ненадежная); уд. в. 7,06; коэф. ЛИН. расширения (при 0°) 0,0000159; коэф. сяшмаемости (при 20°) 0,82-10 см/кг; М. парамагнитен; уд. магнитная восприимчивость 9,66 10 *; уд. теплоемкость (при 0°) 0,1072 са1/г; t° =l 210-1 250° (в зависимости от примесей; чаще всего содержится Fe, Al, Si); теплота плавления 36,7 cal/г; t°Kun. 1 900°. Как элемент марганец отличается переменной валентностью-от 2 до 7. Металлич. М. на воздухе окисляется с поверхности; из разбавленных к-т он легко вытесняет кислород и образует соли двувалентного Мп.>Вода на холоду действует на М. очень медленно, при нагревании-быстрее. М. растворяется в разбавленной соляной кислоте, образуя хлористый марганец, MnClg, и в азотной к-те, образуя нитрат. Холодная конц. HgSOj на М. не действует; горячая- растворяет. М. соединяется непосредственно с фосфором, хлором, бромом, серой, кремнием и углеродом; в парах SOg М. загорается, переходя в сульфат, MnSOj; М. вытесняет многие металлы (мышьяк, сурьму, висмут, олово, медь, цинк) из растворов их солей; сам же М. не вытесняется ни одним металлом. В природе в свободном состоянии М. не встречается, но входит в состав многих минералов, силикатов, руд, гл. обр. железных (см. Марганцевые руды); в незначительном количестве М. находится в почве и естественных водах (в виде бикарбоната); он содержится также в растениях (в семенах й молодых ростках) и в животных организмах (в яичном желтке, волосах, чешуе). Добьшают М. восстановлением его окислов-накаливанием с углем или алюминием (см. Алюми-нометрия). М. легко сплавляется с другими металлами; поэтому его применяют для получения сплавов (см. Манганин, Железо-сплавы); прибавление М. к бронзе (3-6%) придает ей значительную твердость; кроме того М. применяют для восстановления металлов из их окиЬлов (медь, никель). Продажный М. содержит ок. 1% железа, незначительное количество кремния и алюминия. Область технич. применения М. ограничивается его сплавами и металлургией черных п цветных металлов. Чистый М., вследствие его высокой стоимости, почти не имеет промышленного значения. Б. Беркенгейм. Лит.: см. Маргакца соединения. - М. в металлургии играет важную и многообразную роль: 1) являясь всегда составною частью шихты доменньгх печей, он переходит частью (на 50-75%) в чугун, частью в шлак, сообщая последнему жидкоплав-кость, а первому способность выделять серу как в самой доменной печи, так и в миксере (см. Обессериванш миксера); 2) в процессах передела чугуна М. предохраняет железо от излишнего окисления (см. Бессемерование, Томасирование, Мартеновское производство), способствует переходу серы в шлак и своим присутствием в стали парализует вредное влияние остающейся в ней серы; 3) действует как раскислитель на сталь, окисленную в процессе передела, благодаря низкой концентрации в ней углерода и марганца (см. Раскисление); 4) входит в значительном количестве (10--15%) в состав специальных сортов стали, сообщая ей специ-фич. свойства (см. Гадфилъда сталь, Вольфрамовая сталь). Лишь в обычном литейном чугуне содерлсапие М. ограничивается низкими пределами (0,5-0,6%); в гематите допускается 1% его (иногда содержание его доходит до 7%). Передельный чугун содержит не менее 1% М., часто 1,5%, а иногда 2-2,5%, немецкий стальной чугун -до 5%. В растюлители (см.) М. вводится в количестве 20% (зеркальный чугун) или 80% (см. Железосплавы). Вбльшая часть всего М., добываемого в виде руды (см. Марганцевые руды), идет на производство передельного чугуна и раскислителей, значительно меньшая-на изготовление с п е-циальныхсталей. Лит.: Hadfleld R., The Metal Manganese a. Its Properties, Journal of the Iron and Steel Institute*, London, 1927, 1, p. 221-287; Alloys of Iron and Manganese Containing Low Carbon, ibidem, 1927, 1, p. 297-361. M. Павлов. МАРГАНЦА СОЕДИНЕНИЯ. Известны соединения 2-, 3-, 4-, 6- и 7-валентного марганца. Двувалентный ион Мп обнаруживает основные свойства, ион Мп* -слабо основные; четырехвалентный ион Мп б. ч. нейтрален или проявляет слабокислотные свойства; шести- и семивалентный Мп входит в состав кислотных ионов МПО4 и МпО/ и т. о. обладает металлоидным характером. Наиболее устойчивы соединения 2- и 7-валентного Мп, а также окисел четырехвалентного Мп; другие степени валентности Мп б. или м. легко переходят в эти устойчивые формы. Различные степени валентности Мп отличаются и цветом: ион Мп**-розовый, Мп***-тёмнокрасный, МПО4 -зеленый, МпО^-красно-фиолетовый. Ионы двух-, трех- и четырехвалентного Мп проявляют заметную способность к образованию комплексных соединений. Соединения Мп с бором, углеродом, азотом, фосфором, мышьяком и сурьмой обладают ясно выраженными магнитными свойствами. В природе М. с. широко распространены; наиболее крупные их залежи образованы минералами, состоящими из окислов марганца (гл. обр. МпОа) и их гидратов. Другие М.с, гл. обр. соли двувалентного Мп, встречаются в незначительных скоплениях и часто сопровождают природные соединения железа (см. Марганцевые руды). Небольшие количества М. с. всегда содержатся в почве и в золе растений, где они играют повидимому важную роль, входя в состав многих растительных энзимов типа оксидаз. Окислы Мп оказывают на такие энзимы активирующее дейст- вие; так, окислительное действие лакказы пропорционально содержанию Мп в препарате. На активирующем воздействии М. с. на оксидазы основывается повидимому их применение в качестве косвенных (каталитических) удобрений. Каталитич. действие М. с. проявляется и во многих других процессах ферментативного характера, напр. в процессе спиртового брожения. Хорошо известно также применение М. с. в качестве катализаторов в лабораторной и производственной техЕшке (см. Катализ, Катали-тические процессы в технике). Г.т1авная масса добьшаемых М. с. используется в металлургии для получения сплавов марганца и содержащих марганец сортов чугуна и ковкого железа. Кроме того М. с. применяются в стекольном и фарфоровом производствах, в ситцепечатании, для приготовления сикативов, в химическом анализе, при синтезе многочисленных препаратов и т. д. Многие случаи лабораторного и технич. применения М. с. основаны на использованирх их окислительной либо восстановительной способности. При продолжительной работе на производственных предприятиях, в атмосфере к-рых содержится пыль М. с.(иапр. на мельницах для размола MnOj), наблюдаются иногда явления марганцевого отравления (манганизма), выражающиеся в хро-нич. заболеваниях пищеварительных органов и нервной системы. Окислы марганца и их гидраты. Закись марганца, МпО, в природе встречается в виде манганозита. Приготовляется б. ч. прокаливанием в токе водорода других окислов Мп, а также его углекислой или свежеосажденной щавелевокислой соли. МпО-аморфный порошок зеленого цвета; при нагревании без доступа воздуха он становится бледножелтым. При прокаливании исходных веществ в атмосфере смеси водорода с хлористым водородом МпО получается в виде прозрачных зеленых кристаллов правильной системы, с алмазным блеском, уд. в. 5,091, плавяпщхся при *° белого каления. На воздухе МпО (особенно в виде порошка) уже при обыкновенной окисляется, а при нагревании воспламеняется, превращаясь в МП3О4. В химическом отношении МпО обладает основными свойствами; в кислотах легко растворяется, образуя соли двувалентного Мп; при нагревании в атмосфере SOa превращается в закисную сернокислую соль Мп. Восстановление МпО до металлич. марганца водородом происходит только при 2 500°. При сплавлении МпО с металлич. алюминием над известью и плавиковым шпатом получается довольно чистый (до 97% Мп) металлич. марганец. Гидрат закиси марганца, Mn(OH)g, в природе встречается в виде п ир охр опта; приготовляется осаждением из солей двувалентного Мп едкими щелочами. В свежеосажденном состоянии-аморфный белый порошок, который на воздухе быстро буреет вследствие окисления; при высушивании на воздухе переходит в закись-окись марганца. При определенных условиях Мп(0Н)2 м. б. получен в кристаллической (гексагональные призмы), а также в коллоидальной форме. Окись марганца, бурая окись мар- ганца, МП2О3 (или МпО МпОа), в природе встречается в виде браунита. Получается б. ч. прокаливанием на воздухе MnOgHсолей А1 с азотной или щавелевой к-тами; тем-нобурый или черный порошок, уд. в. 4,32;. 1°пл. ок. 700°; до 940° MngOg постоянна, выше этой f переходит с выделением кислорода в МП3О4. Водородом при красном калении восстанавливается в МпО; под действием сероводорода превращается в MnS. Окись марганца обладает слабоосновным характером; с ра,збавленными HgSO и HNO3 она дает МпОа и соли Мп ; с конц. H2SO4 и НС1 на холоду образует соли Мп *, а при нагревании-соли Мп** при выделении кислорода или хлора. Применяется как керамическая краска. Гидрат, окиси марганца,Мп(ОН)з, образуется в виде красно-бурого осадка при действии воздуха на аммиачные растворы солей Мп** в присутствии солей аммония. Он очень непрочен и легко теряет воду, переходя в более постоянный неполный гидрат Мп202(ОН)2 или MngOg HgO, встречающийся в природе в виде манганита. Этот гидрат получают пропусканием хлора в водную суспензию MnGOg; он получается также из раствора MnClj (при производстве хлора по способу Вельдона) осаждешшм едким натром и последующим окислением выпавшего осадка на воздухе либо действием на раствор MnCla хлорной извести и других окислителей; осадок Мп202(ОН)2 промывается разбавленной H2SO4 или HNO3 и водой. Искусственно полученный МПаОз HjO - аморфный или микрокристалл1шеский порошок коричневого или серостального цвета, оттенки которого зависят от способа получения; при нагревании выше 110° гидрат медленно теряет воду, переходя в MnaOj. Применяется как краска под названием марганцевого, или минерального, бистра (см. Марганцевые краски. Бистр, Краишше), а также в качестве сикатива. Закись-окись марганца, красная окись марганца, МпдОл, в природе встречается в виде гаусманита. Получается при прокаливании всех других окислов марганца на воздухе и весьма постоянна; поэтому при весовом анализе М. с. Мп определяется обычно в виде МП3О4. В зависимости от способа получения МП3О4 бьшает аморфной или кристаллической. Цвет ее б. ч. темно-красный, переходящий при нагревании в черный; уд. в. 4,653-4,748. Двуокись марганца, перекись марганца, МпОа, в природе встречается в значительных количествах в виде пиролюзита и полианита, а также в составе разных видов вада (см.). Искусственно MnOg получается из низших окислов или солей Мп путем перевода их в азотнокислую соль, которая затем окисляется азотной к-той совместно с бертолетовой солью или без последней. При получении хлора по способу Вельдона расходуемая в процессе МпОа регенерируется путем продувания воздуха при 55-60° через раствор MnClg (отход производства), обработанный избытком гашеной извести. В 1929 г. Като и Мацугуси предложили новый способ приготовления МпО^, основанный на окислении низших: окислов марганца в присутствии небольшого количества ш^елочей (напр. 5%) в токе воздуха при 400-500°; окисление при этих условиях происходит почти моментально. MnOg образуется также на аноде при электролизе растворов солей Мп. Искусственно полученная MnOg-черный кристаллич. порошок, со-стояпдий из микроскопич. стально-серых табличек, в очень тонких слоях просвечиваю-пщх пурпурно-красным цветом; под давлением приобретает металлич. блеск; обладает значительной электропроводностью. По химическому характеру MnOg являетсяамфо-терным окислом, с преобладанием сла'Ьокис-лотньЕХ свойств; она имеет нормальное строение О : Мп : О (поэтому название перекись марганца неправильно). Чистая HNO3 не действует на MnOg, но в присутствии N0 или органич. восстановителей (щавелевой кислоты, сахара и т. п.) происходит образование Мп(ЫОз)а. При действии концентрированной HaSOi образуется сперва Mna(S04)8i а затем MnS04, причем наделяется половина кислорода, содержащегося в MnOj: Мп Оа + HgSOi = MnS О4 + HjO 4- о. При действии крепкой НС1 при нагревании происходит образование MnClg и выделение хлора; на этой реакции основывалось техническое получение хлора по способу Вельдо-на. При действии SOg на тонкоизмельченную МпОа при слабокрасном калении образуется в качестве конечного продукта MnS. При сплавлении МпОз с КОН происходит образование KgMnOi. В кислой среде MnOg является довольно энергичным окислителем; во многих случаях МпОз обнаруживает ка-талитическ. действие; напр. она активирует разложение бертолетовой соли, получение мочевины из цианалшда кальция, окисление СО в COg и т. д. В технике MnOj применяется б. ч. в В1вдв природного пиролюзита и других содержащих МпОа минералов. Наибольшие количества МпОа идут на приготовление различных сортов чугуна, стали и сплавов марганца. В стекольном npOHBBOJa;-стве МпОа служит для придания стеклу аметистового или (при содержании МпОа До 6-7%) черного цвета. При нагревании стеклянной массы в печах MnOg разлагается по ур-иям: ЗМп02= Mns04 + О2; Мп804 = МпаОз + МпО. В небольших количествах МпОа прибавляют в стекло и глазури с целью уничтожения зеленоватого оттенка, придаваемого стеклу солями закисного железа; при этом обесцвечивание происходит отчасти вследствие окисления закисных солей железа в окисные, отчасти благодаря дополняющему действию окраски соединений Мп на окраску силикатов железа. Далее МпОа применяется: при изготовлении глазурей и эмалей черного, темнофиолетового, металлич. и синего цвета, служащих для покрытия глиняной посуды и железных изделий; в качестве краски под названием марганцевой черной и как исходный материал для пол^чения марганца и всех М. с. МпОа находит применение также при синтезе некоторых органич. красителей (напр. при окислении лейкосоединений, при получении пурпурина из ализарина); MnOg является одним из наиболее сильных сикативов для высыхающих масел; в небольших количествах МпОа иногда прибавляется к каучуку для улучшения его свойств. В тонко-измельченном виде МпОа служит для удаления из воды соединений железа. Электролитич. MnOg применяется для воронения стволов огнестрельного оружия. Наконец МпОа употребляется в качестве деполяризатора в гальванич. элементах Лекланше и служит для приготовления анодов, применяемых в электролизе. Гидрат двуокиси марганца, MnOa-aq, в природе встречается в виде ц с н-ломелана. Получается он окислением МпаОз, МП3О4, Мп(0Н)2 и солей Мп различными окислителями (HNOe, HNOg-l-KClOa, хлором, солями хлорноватистой и бромнова-тистой к-т и др.), а также восстановлением раствора КМПО4 (щавелевой к-той, MnSO* и др.). Можно перевести MnOg в гидрат, нагревая ее под давлением со щелочами []. МпОа aq - рьЕклый порошок темнобурого или черного цвета; уд. в. ок. 2,58; содержание в нем воды непостоянно и зависит от способа приготовления. При высушивании над HaSOa гидрат теряет воду очень медленно; полного обезвоживания путем нагревания достигнуть не удается вследствие начинающегося разлонсения окисла. МпОа aq обладает явно кислотными свойствами; с гидратами щелочных и щелочноземельных металлов образует м а н г а и иты-соединения типа МСаМпОз.где Me-одновалентный катион; из карбонатов MnOa-aq выделяет COg. Применяется в тех же случаях, как и безводная MnOg, причем окислительные свойства у гидрата выражены сильнее. В последнее время разрабатьшаются способы использования МпОа aq для очищения сернокислого алюминия от примеси железных солей (FeSO), с чем связана возможность производства чистых гидроокиси и сульфата алюминия из обыкновенных глин; метод основан на адсорбирующей способности MnOg-aq.-Коллоидная двуокись марганца получается б. ч. из КМПО4 действием органич. восстановителей (с1-глюкозы, левулозы, галактозы, гуммиарабика) в разбавленных растворах едких щелочей или крепкого раствора аммиака (прибавляется по каплям к кипящему 0,05 N раствору КМПО4), а также раствора перекиси водорода. МпОа aq, полученная при кипячении МПаОв и МП3О4 с HNO3, после удаления кислоты также легко переходит в коллоидальное состояние. Гидрозоль MnOg-aq- прозрачная жидкость желтого или бурого цвета; большая часть электролитов (кроме КМпОа) вызывает его коагуляцию. Марганцовистый ангидрид, МпОз. Существование этого окисла, равно как и его гидрата-свободной марганцовистой кислоты, Н3МПО4,-нельзя считать вполне установленным. Марганцевый ангидрид, семи-окись марганца, МпаО получается осторожным нагреванием до 60-70° полученного на холоду желтовато-зеленого раствора KMnOj в слегка разбавленной серной к-те (0,5 мол. НаО на 1 мол. HgSOi) и конденсащгей выде-ляюпщхся фиолетовых паров или осторожным растиранием смеси 25 - 50 см чистой конц. H2SO4 с 25-50 г совершенно чистого KMnOi и отделением получающихся маслянистых капель. MngO,-густая зеленовато-черная (или желто-зеленая) маслянистая жидкость, уд. в. 2,4. Самопроизвольно разлагается на воздухе, вьщеляя сильно озонированный кислород,и обладает сильнейшими окислительными свойствами. При соприкосновении с МпаО, многие органич. вещества (бумага, спирт, эфир, светильный газ и т. д.) воспламеняются. При быстром нагревании до 45° (а иногда и при обыкновенной t°) МП2О7 сильно взрывает. Марганцевая кисл ота,НМп04,м.б. получена только в виде растворов не выше 20%-ной концентрации. При выпаривании раствора на холоду м. б. вьщелен твердый гидрат марганцевой к-ты, НМПО4 п Н2О, в виде красновато-бурых кристаллов. Раствор НМПО4 легко разлагается при стоянии или слабом нагревании, выделяя MnOg, эта реакция используется иногда для получения препаратов МпОа с большой каталитической активностью. Марганцевая кислота в растворах сильно ионизирована и имеет характерный спектр поглощения (принадлежащий иону MnOiO с 5 абсорбционными полосами в зеленой части. Соли двувалентного Мп. Получаются при действии кислот на металлич. марганец, на карбонат MnCOg и на все окислы Мп, причем из высших окислов выделяется кислород, а в случае соляной к-ты-хлор. Большинство растворимых солей Мп , независимо от содержания в них кристаллизационной воды (от О до 9 молекул),-светлорозо-вого цвета; исключением является -роданид марганца, Mn(CNS)2, желтый в безводном состоянии, зеленый в виде гидрата и розовый в растворе. Нерастворимые соли Мп -белого цвета; соли слабых к-т темнеют на воздухе вследствие окисления; соли сильных к-т на воздухе не изменяются. Большинство солей Мп хорошо растворимы в воде и образуют ряд кристаллогидратов; многие из них принимают участие в образовании двойных солей и комплексных соединений (благодаря образованию комплексных соединений аммиак при действии на растворы солей Мп в присутствии NH4CI не осаждает гидрата закиси марганца). Ацетат марганца, уксуснокислый марганец, Мп(С2Нз02)а 4 HgO, получается действием уксуснокислого бария или свинца на MnS04. Герм, способ производства [] состоит в нагревании при 80° пиролюзита с конц. уксусной к-той при постепенном добавлении ацетальдегида; последний, восста-новляя МпОа ДО МпО, сам окисляется в уксусную к-ту, к-рая идет на образование ацетата. Ацетат Мп-постоянные на воздухе бледнокрасные таблички ромбич. или моно-клинич. системы. Уц. вес четырехводной соли 1,589, безводной-1,745. Растворимость: 1 ч. в 3 ч. холодной воды и в 3,5 ч. спирта. Применяется в качестве сикатива, катализатора для кислородных ванн и каталитич. удобрения. Бораты марганца, борнокислые соли Мп. Тетраборат марганца, МПВ4О, 5 HgO, получают осайсдением раствора 1 моля буры и 2 молей NaOH при помощи раствора 2 молей MnCla и дальнейшим сплавлением полученного т. о. осадка [состава МпН4(ВОз)а- HgOJc борной кислотой в количестве, необходимом для получения вещества с ф-лой Mn()-2B20g. Белый порошок; на воздухе постоянен. Метаборат марганца, Мп(В02)22 Н2О, получается путем взаимодействия раствора буры с какой-нибудь солью Мп ; белый порошок, нерастворимый в воде. Обыкновенный продажный борат марганца не представляет определенного соединения, содержит 37-1 % В2О3 и 12-31% МпО. Для его получения обрабатьшают раствор MnClg, остающийся от добьшания хлора по способу Вельдона, сперва известковым молоком (для удаления Fe) и затем небольшим избытком буры при нагревании; к осадку прибавляют раствор аммиака (уд. веса 0,960), затем его отжимают, высушивают и просеивают. На воздухе продукт быстро окисляется и темнеет; чтобы помешать этому, к нему часто прибавляют MnSOi, что однако ведет к образованию в дальнейшем сероводорода. Борат Мп находит ши*рокое применение в качестве сикатива; применяется также в качестве катализатора в кислородных ваннах. Хлористый марганец, MnCla, в технике получался гл. обр. из жидкости, остающейся от получения хлора действием НС1 на МпОа- По другому способу его приготовляют, растворяя марганцевую руду в НС1, вьшаривая раствор, осторожно прокаливая остаток в тигле, извлекая его водою и сгущая полученный раствор до кристаллизации. Обычно в технике применяют тетра-гидрат, MnClg 4Н2О, - розовые гигроскопические распльшаюпщеся таблички уд. веса 1,913. При 100° тетрагидрат теряет 3 мол. воды, а при 200-230° начинает выделять хлор, не теряя остатка воды. В 100 ч. воды растворяется следующее количество соли: при 8° 31,25° 62,5° 87,5° 106,25° 151 Ч. 265 Ч. 641 Ч. 641 Ч. 656 Ч. Безводный MnCla-бледнорозовая кристаллич. масса с i° , 650° и уд. в. 1)2в = 2,977. В 100 ч. воды растворяется соли: при 10° 31,25° 62,3° 87,5° 106,2° 62,16 Ч. 85,72 Ч. 122,22 Ч. 122,22 Ч. 123,81 Ч. В соляной к-те MnClg растворяется хуже чем в воде; растворим в спирте, метиловом спирте и ацетоне; в эфире не растворяется. Легко образует двойные соли, как например MnCla - 2NH4CI НаО. Хлористый Мп применяется для окрашивания тканей в прочный коричневый цвет (марганцевый бистр), частью для изготовления других М. с, как каталитич. удобрегше и т. д. Присутствие примесей сильно понижает технич. пригодность MnCla: напр. содержание более 1% CaClg делает его непригодным для ситцепечатания. Карбонат марганца, углекислый марганец, MnCOg. Встречается в природе в виде марганцевого шпата; искусственно получается осаждением из раствора MnCla содой. Белоснежный тонкий порошок уд. веса 3,13; на воздухе не изменяется. Всегда содержит большее или меньшее количество воды, к-рую начинает терять при 70°. Разлагается при 250-300° с образованием МпО, а затем MngOg; при сильном прокаливании образует МП3О4. Очень плохо растворим в 1 ... 23 24 25 26 27 28 29 ... 48 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
© 2007 SALROS.RU
ПромСтройМат |